题目内容
【题目】实验一:根据下图回答问题。
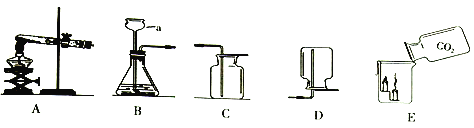
(1)仪器a的名称是__________。
(2)实验室用大理石和稀盐酸制取二氧化碳化学方程式为_________________________,选用的收集装置____________。
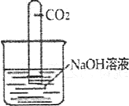
(3)图E所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛现象是________________________,产生该现象的化学原因是____________________。
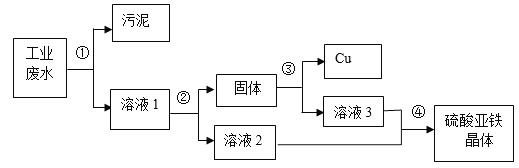
实验二:已知Fe2O3样品中含有杂质FeS2.兴趣小组用下图装置测定样品中FeS2含量。称取mg样品置于玻璃管Y内。充分灼烧该样品,根据实验后装置Z增加的质量推算FeS2质量(装置管内发生反应:4FeS2+11O2![]() 2Fe2O3+8SO2)
2Fe2O3+8SO2)

(4)连接好仪器,检查整套装置的气密性:在装置Z中加水至浸没长导管末端,关闭开关b,加热玻璃管Y,观察到___________________,说明装置气密性良好。
(5)使用“实验一 ”装置B制得的氧气进行实验,装置X瓶内需盛放的干燥剂是________________。
玻璃管Y内反应完全后,停止加热,若立即停止通入氧气,会导致误差,其原因是___________。
(6)若将通入的氧气改为空气进行同样的实验(样品反应完全),则测得FeS2含量__________(选填“偏大”“偏小”或“无影响”)数据。
【答案】 长颈漏斗 CaCO3+2HCl=CaCl2+H2O+CO2↑ c 自下而上熄灭 不具助燃性和可燃性 z中有气泡产生 浓硫酸 Z中有外界二氧化碳进入与氢氧化钠反应 偏大
【解析】(1)a仪器是长颈漏斗;
(2)碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;密度比空气大,能溶于水,因此只能选C收集;(3)向盛有阶梯蜡烛的烧杯中倒入二氧化碳,可以观察到下层的蜡烛火焰先熄灭,上层的蜡烛火焰后熄灭;由此可知二氧化碳具有的性质是密度比空气大,不能燃烧、不能支持燃烧;
(4)检查整套装置的气密性:在装置Z中加水至浸没长导管末端,关闭开关b,加热玻璃管Y,观察到:装置乙处导管口有气泡冒出,停止加热后一段时间,长导管内液面上升;
(5)氧气可以用浓硫酸干燥,玻璃管Y内反应完全后,停止加热,若立即停止通入氧气,会导致误差,其原因是:生成的气体没有全部被吸收;
(6)若将通入的氧气改为空气进行同样的实验(样品反应完全),则测得FeS2含量偏大,因为空气中的二氧化碳与氢氧化钠反应,装置Z增加的质量偏大。

 阅读快车系列答案
阅读快车系列答案【题目】实验室用石灰水而不用氢氧化钠溶液鉴定二氧化碳。氢氧化钠能否与二氧化碳反应?
【查阅资料】Ⅰ.氢氧化钠溶液与二氧化碳反应生成易溶的碳酸钠,碳酸钠在二氧化碳过量的条件下继续与水和二氧化碳反应生成碳酸氢钠
Ⅱ.碳酸钠和碳酸氢钠性质对比如下表
操作 | NaHCO3溶液 | Na2CO3溶液 |
加入稀盐酸 | 产生气泡 | 产生气泡 |
加入稀CaCl2溶液 | 无明显变化 | __________________(填写现象)) |
加热溶液至沸腾,并将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
【进行实验】
实验操作 | 实验现象 | 结论及化学方程式 |
| ___________________ | 氢氧化钠与二氧化碳反应生成碳酸钠.反应方程式_______________ |
【实验反思】学习小组讨论,认为产生此实验现象的原因可能有两种:一种是NaOH与C02发生了反应;另一种是_______________
(2)为了进一步验证CO2与NaOH溶液已经发生反应,请你设计一个简单的实验检验生成的新物质。
实验步骤 | 实验现象 | 解释与结论 |
____________________________ | ____________________________ | NaOH与CO2发生了反应 |
【实验拓展】该小组同学将二氧化碳通入氢氧化钠溶液中,利用数字化技术测定溶液pH值变化,待完全反应后,观察到溶液中逸出大量气泡,pH出现两段S型变化曲线。

【实验分析】
(3)AB段变化的原因可能是________。BC段变化的原因可能是___________。利用实验验证变化后的产物,实验操作为_________________.实验现象是____________________。