题目内容
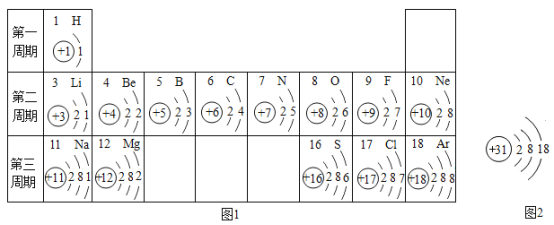
【题目】(1)分类是学习和研究物质性质常用的一种方法,物质的性质决定物质的用途。按要求从硫酸、氮气、盐酸、氯化银、氢氧化铜、甲烷中选择合适的物质,将其化学式填写在下列横线上。
①最简单的有机物________________;
②可作食品袋填充气体的单质____________________;
③一种难溶性的碱________________;
④一种易挥发的酸____________。
(2)全球首创的智能共享摩拜单车正式登陆泉城济南,为市民提供出行服务,倡导绿色出行,共建美好城市。
①摩拜单车从骑行安全因素考虑,车身的材料使用了铝合金。铝合金材料的车身具有不易被腐蚀,不易被损坏等优点,可以延长单车的使用寿命。铝合金属于__________________(填写“金属材料”“复合材料”“有机高分子材料”之一)。
②摩拜单车的轮胎使用无毒环保橡胶制作,采用“横向镂空”设计,具有缓冲好、不怕扎、免充气及可回收再利用等众多优点,是国家提倡的“绿色环保”产品。已知合成橡胶是由不同单体在引发剂作用下,经聚合而成的品种多样的高分子化合物。单体有丁二烯、苯乙烯、丙烯腈等多种。其中丙烯腈(CH2CHCN)中碳、氢元素的质量比为_______________(填最简整数比)。
③摩拜单车的入驻解决了济南市民出行“最后一公里”的问题,减少了私家车的使用。私家车尾气的大量排放是导致酸雨的重要原因,请简述酸雨的形成过程_______________。
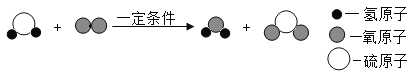
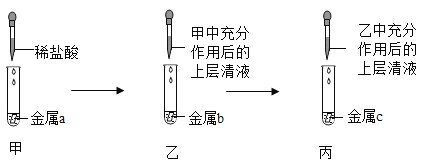
(3)为减少CO2在空气中的排放量,实际生产中,经常利用NaOH溶液来“捕捉”CO2,流程如下图(部分条件及物质未标出)。
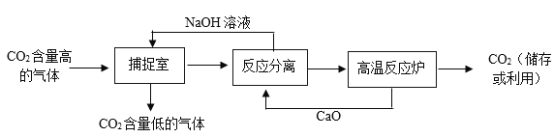
①捕捉室内发生的化学反应的化学方程式为________________;
②“高温反应炉”内发生的反应为________________反应(填“化合”“分解”“置换”“复分解”之一)。
【答案】CH4 N2 Cu(OH)2 HCl 金属材料 12:1 汽车尾气中的二氧化硫与氮氧化物与大气中的水蒸气发生化学反应生成酸,随雨水降落到地面,形成酸雨 CO2+2NaOH=Na2CO3+H2O 分解
【解析】
(1)①甲烷是结构最简单的有机物;故填:CH4;
②氮气的化学性质不活泼,可以填充食品包装袋内做保护气;故填:N2;
③氢氧化铜是一种蓝色的难溶性碱;故填:Cu(OH)2;
④盐酸是一种具有挥发性的酸;故填:HCl;
(2)①金属材料包括纯金属与合金,所以铝合金属于金属材料;故填:金属材料;
②丙烯腈(CH2CHCN)中碳、氢元素的质量比为(12×3):(1×3)=12:1;故填:12:1;
③汽车尾气中的二氧化硫与氮氧化物与大气中的水蒸气发生化学反应生成酸,随雨水降落到地面,形成酸雨;故填:汽车尾气中的二氧化硫与氮氧化物与大气中的水蒸气发生化学反应生成酸,随雨水降落到地面,形成酸雨;
(3)①捕捉室中发生反应的化学反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,其化学方程式为CO2+2NaOH=Na2CO3+H2O;
故答案是:CO2+2NaOH=Na2CO3+H2O;
②高温反应炉是碳酸钙高温分解生成氧化钙和二氧化碳,属于分解反应;
故填:分解。

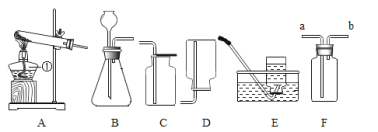
【题目】同学们在初中化学实验室中,发现一瓶如图所示久置的瓶口有白色固体、瓶塞丢失的无色溶液。已知原溶液可能是NaCl、NaOH或Na2CO3三种溶液中的一种,为确定溶液成分,同学们进行了如下探究:
![]()
(1)探究成分
①小张同学取待测液测得pH=10,他得出的溶液中一定不含_______。他取少量待测液于试管中,加入过量的稀HCl,看到______,由此小张同学认为,溶液为Na2CO3溶液。
②小李同学对小张同学的结论提出疑问,拟进行以下实验:取少量待测液于试管中,加入过量的BaCl2溶液,生成白色沉淀,该反应方程式为_______,过滤,取滤液,(写出还需进行的操作及现象)________________。通过实验,小李认为小张结论不正确。
③同学们通过讨论认为试剂瓶原标签应该是氢氧化钠,但因吸收空气中 _____的而变质。
(2)测定碳酸钠的浓度
取该试剂瓶中溶液50g倒入烧杯中,再向烧杯中逐滴滴加盐酸使其充分反应至无气泡产生(假设生成的二氧化碳全部逸出)。测得加入盐酸的质量与烧杯中的物质的质量关系如下表所示。
累计加入盐酸的质量/g | 0 | 25 | 37.5 | 50 |
烧杯中物质的总质量/g | 50 | 75 | 85.3 | 97.8 |
请你计算:①这一测定过程中产生二氧化碳质量为___g。
②这一瓶试剂中碳酸钠的质量分数___(写出计算过程)。