题目内容
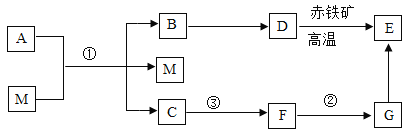
【题目】以氢氧化钠溶液为例的反应关系(如下图)体现了碱类物质的化学性质,结合此图回答下列问题:
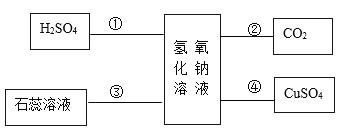
(1)反应①中若 H2SO4 与 NaOH 恰好完全反应,溶液的 pH___________7(填“>”、“<”或“=”);为验证性质③将氢氧化钠溶液滴入紫色石蕊溶液中,溶液颜色由紫色变成_________________。
(2)写出反应④的化学方程式__________________。
(3)写出图中发生中和反应的化学方程式_________________。
【答案】= 蓝色 ![]()
![]()
【解析】
(1)反应①中H2SO4与NaOH恰好完全反应生成硫酸钠和水,硫酸钠溶液为中性,溶液的pH=7;碱溶液能使紫色石蕊试液变蓝;
(2)反应④是硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为 CuSO4+2NaOH═Cu(OH)2↓+Na2SO4;
(3)图中硫酸与氢氧化钠反应生成硫酸钠和水属于中和反应,化学方程式为 2NaOH+H2SO4=Na2SO4+2H2O。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
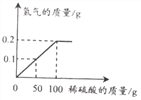
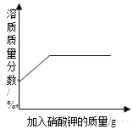
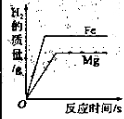
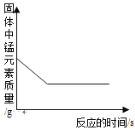
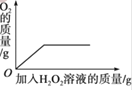
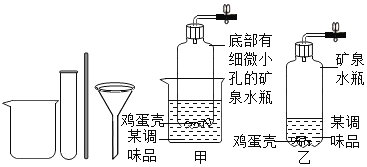
【题目】下列图像能正确反映对应变化关系的是( )
|
|
|
|
A.20℃时,向一定量的硝酸钾不饱和溶液中加入硝酸钾固体 | B.将等质量的镁片和铁片投入到足量稀硫酸中 | C.用酒精灯加热一定量的高锰酸钾固体 | D.向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液 |