题目内容
【题目】铜锌合金又称假黄金。向盛有30g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢的质量与加入稀硫酸的质量关系如右图所示,计算:
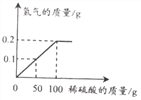
(1)充分反应后生成氢气的质量为___________g。
(2)合金样品中锌的质量为_________。
(3)恰好完全反应时,所得溶液溶质的质量分数为_________。(结果保留一位小数)
【答案】 0.2 6.5g 15.1%
【解析】(1)由图中信息知,充分反应后生成氢气的质量为0.2g。
(2)解∶设合金样品中锌的质量为x,反应生成硫酸锌质量为y
Zn+ H2SO4 == ZnSO4 + H2↑
65 161 2
x y 0.2g
![]() =
=![]() ,x=6.5g;
,x=6.5g;![]() =
=![]() ,y=16.1g。
,y=16.1g。
(3)恰好完全反应时,所得溶液溶质的质量分数为∶![]() ×100%=15.1%。
×100%=15.1%。
点睛∶正确书写化学方程式,并根据化学方程式进行简单计算是顺利完成本题的重要保证。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目