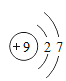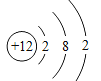题目内容
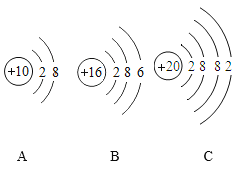
【题目】在实验探究课上,化学老师给了同学们一包红色粉末,该粉末是由Cu 、Fe2O3 、Fe(OH)3三种固体中的一种或两种组成,其中一个小组同学提出如下猜想并进行探究:
(提出猜想)红色粉末可能的组成有:
只有Fe2O3
②是Cu 、Fe2O3的混合物
![]() ③是Fe2O3 、Fe(OH)3的混合物
③是Fe2O3 、Fe(OH)3的混合物
(查阅资料)(1)2Fe(OH)3 Fe2O3 +3H2O
(2)无水CuSO4白色固体遇水变蓝
(3)Cu在FeCl3溶液中发生的反应:2FeCl3+Cu 2FeCl2+CuCl2
(实验探究)
(1)甲同学取适量红色粉末装入试管中,按图11进行实验,结果无水CuSO4没有变蓝,从而排除猜想中的 (填猜想中的序号)。
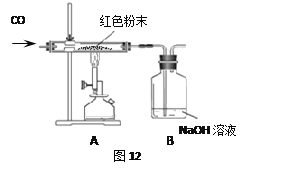
(2)乙同学为进一步确定红色粉末的组成,按图12称取少量红色粉末放入硬质玻璃管中,通入CO片刻,然后加热至完全反应,停止加热,继续通入CO冷却至室温。

(反思评价)
(1)实验时通入CO片刻后再加热的原因是 。
(2)实验过程中,A装置中发生反应的化学方程式是 。
(3)从环保角度看,图12装置存在的不足之处是: 。
(4)如果观察到A装置中红色粉末部分变黑,则猜想 正确(填序号)。
(拓展延伸)丙同学认为:在甲同学实验结论的基础上,还可以这样探究猜想①和②。取少量红色粉末于试管中,滴加足量稀盐酸,振荡后发现固体全部溶解,溶液变色,即可以排除猜想中的②。你认为丙同学的观点是否正确? (填“正确”或“不正确”),理由是
【答案】【实验探究】(1)③
【反思与评价】(1)防止玻璃管中的CO与空气混合受热发生爆炸(或其他合理答案均得分) (2)3CO+Fe2O3![]() 2Fe+3CO2 (3)没有进行尾气的处理 (4)②
2Fe+3CO2 (3)没有进行尾气的处理 (4)②
【拓展延伸】不正确、Fe2O3与盐酸反应得到FeCl3溶液,Cu又与生成的FeCl3反应得到FeCl2和CuCl2溶液(或Fe2O3+6HCl=2FeCl3+3H2O,2FeCl3+Cu = 2FeCl2+CuCl2)
【解析】
本题是一道综合性探究题,利用物质的性质不同设计实验加以甄别,来探究红色粉末的组成,先分别探究其中是否含有Fe(OH)3、Fe2O3、Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究确定其组成.
根据【资料获悉】中的(1)(2)(3)和探究(1)可排除猜想中的③.
【反思评价】要考虑到CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此,应先通CO排尽玻璃管中的空气,然后再加热.应考虑到CO有毒,排放到空气中会污染大气,显然,该装置没有对尾气进行处理.在探究的同时也出现了与上述高考题中相同的防倒吸及尾气处理等考点.同时考查了一氧化碳还原氧化铁的实验操作要点实验现象等,对氢气的还原性也进行了衍生.
解答:解:【实验探究】
(1)根据资料 2Fe(OH)3![]() Fe2O3+3H2O,白色无水CuSO4遇水变蓝;加热红色粉末,结果无水CuSO4没有变蓝,从而排除猜想中的含有Fe(OH)3的选项③;
Fe2O3+3H2O,白色无水CuSO4遇水变蓝;加热红色粉末,结果无水CuSO4没有变蓝,从而排除猜想中的含有Fe(OH)3的选项③;
【交流讨论】
根据CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此,应先通CO排尽玻璃管中的空气,然后再加热.所以在装置A中先通CO气体的作用是:排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸);故答为:
(1)实验时通入CO片刻后再加热的原因是:防止玻璃管中的CO与空气混合受热发生爆炸.
(2)实验过程中,A装置中发生反应的化学方程式是:3CO+Fe2O3![]() 2Fe+3CO2.
2Fe+3CO2.
(3)从环保角度看,图12装置存在的不足之处是:没有进行尾气的处理.
(4)如果观察到A装置中红色粉末部分变黑,则猜想:②正确.
【拓展延伸】丙同学认为:在甲同学实验结论的基础上,还可以这样探究猜想①和②.取少量红色粉末于试管中,滴加足量稀盐酸,振荡后发现固体全部溶解,溶液变色,即可以排除猜想中的②.则丙同学的观点不正确,理由是:Fe2O3与盐酸反应得到FeCl3溶液,Cu又与生成的FeCl3反应得到FeCl2和CuCl2溶液(或Fe2O3+6HCl=2FeCl3+3H2O,2FeCl3+Cu=2FeCl2+CuCl2).
故答为:【实验探究】(1)③
【反思与评价】(1)防止玻璃管中的CO与空气混合受热发生爆炸(或其他合理答案均得分)
(2)3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
(3)没有进行尾气的处理
(4)②
【拓展延伸】不正确、Fe2O3与盐酸反应得到FeCl3溶液,Cu又与生成的FeCl3反应得到FeCl2和CuCl2溶液(或Fe2O3+6HCl=2FeCl3+3H2O,2FeCl3+Cu=2FeCl2+CuCl2)

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案【题目】盐酸溶液中含有H2O分子、H+和Cl-,要探究是哪一种粒子能使紫色石蕊溶液变成红色,请观察在白色点滴板上进行的下列实验,将实验现象和结论填入下表。

滴加紫色石蕊溶液后的现象 | 结论 | |
第1孔 | 孔中溶液仍为紫色 | 水分子_________________ |
第2孔 | ____________________ | _______________________ |
第3孔、第4孔 | ____________________ | _______________________ |
【题目】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
(查得资料)
(1)该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
(2)饱和碳酸氢钠溶液不吸收二氧化碳。
(3)碱石灰的主要成分为氧化钙和氢氧化钠。
(设计实验)小组同学设计了如图所示装置(图中夹持仪器略去)测定牙膏样品中碳酸钙的含量。
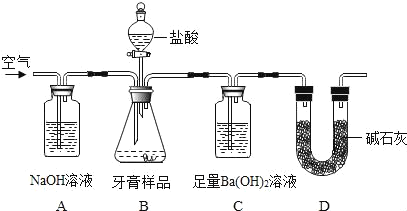
依据图示回答下列问题:
(1)B装置使用分液漏斗的优点是_____。
(2)A中氢氧化钠溶液的作用是_____。
(3)C中观察到有沉淀产生,反应的化学方程式为_____。
(4)实验过程中需持续缓缓通入空气,其作用有_____。
(解释与结论)将C中产生沉淀通过_____、洗涤、干燥、称量,通过计算求得牙膏样品中碳酸钙的含量。
(反思与评价)
反思实验过程,小刚同学提出应采取必要措施,提高测定准确度。他提出的下列各项措施中,不能提高测定准确度的是_____(填字母序号)。
a 在加入盐酸之前,排净装置内的CO2气体
b 放慢滴加盐酸的速度
c 在A﹣B之间增添盛有浓硫酸的洗气装置
d 在B﹣C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(拓展延伸)小亮同学为确定A中溶质成分,进行了如表所示实验:
实验操作 | 实验现象 | 实验结论 |
(1)、取少量滤液于试管中,加入足量____ | 产生白色沉淀 | 溶质主要成分为Na2CO3和NaOH |
(2)、过滤,取少量滤液加入 | _____ |