题目内容
【题目】我们生活在丰富多彩的物质世界中,人类的生产、生活离不开化学。
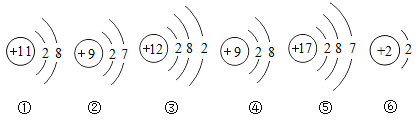
(1)用适当的化学用语填空:空气中最多的气体________ ;保持氧气化学性质的微粒_______;氧化镁中氧元素化合价为-2价________;含氧量最高的氧化物__________。
(2)选择下列适当的物质填空(选填序号):
A干冰 B明矾 C石墨 D硫酸亚铁
(1)可用来治疗贫血的是__________;
(2)常用作电池电极的是__________;
(3)可用于人工降雨的是__________;
(4)常作净水剂的是_____________;
【答案】N2 O2 ![]() H2O2 D C A B
H2O2 D C A B
【解析】
()空气中含量最多的气体是氮气,约占78%;氧气由氧分子构成,因此保持其化学性质的最小微粒是氧分子,填O2;氧化镁中氧元素化合价为-2价,![]() ;含氧量最高的氧化物是过氧化氢,填H2O2。
;含氧量最高的氧化物是过氧化氢,填H2O2。
(2)①人体缺少铁元素可能导致缺铁性贫血,选D;②石墨具有优异的导电性,故可做电极材料,答案选C;③干冰升华吸热,因此可用于人工降雨,选A;④明矾投入水中,可吸附悬浮小颗粒使其聚沉,故作净水剂,选B。

【题目】催化剂在生产、生活和科研中的地位越来越重要。
探究一:验证MnO2在过氧化氢分解前后的质量没有改变。
某同学用电子天平称取1.0gMnO2于试管中,加入适量过氧化氢溶液,写出发生反应的化学方程式_____________。反应结束后,过滤、洗涤、称量,发现所得固体质量大于1.0g,其可能原因是____________。小强针对上述原因提出烘干后再称量的方案,结果得到了准确的实验结果。
探究二:温度对过氧化氢反应速率的影响。
某同学用如图所示装置进行实验,发现加热后产生气泡速率明显加快,但用带火星的木条检验产生的氧气时,木条很难复燃,其可能原因是____________。
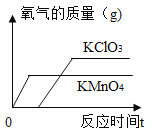
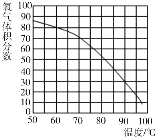
经实验测定,受热液体的温度与得到氧气的体积分数之间存在一定关系(如图所示)。若能使带火星木条复燃所需氧气的体积分数最低为49%(只考虑氧气的体积分数对实验结果的影响),现欲使带火星的木条复燃,应将加热过氧化氢溶液的最高温度控制在_________ ℃以下。
探究三:红砖粉是否也能作过氧化氢分解的催化剂?效果怎样?
小雨以收集等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
编号 | 过氧化氢 | 其他物质 | 待测数据 |
实验1 | 20mL 5% 过氧化氢溶液 | 无 | |
实验2 | 20mL 5% 过氧化氢溶液 | 1g红砖粉 | |
实验3 | 20mL 5% 过氧化氢溶液 | 1g二氧化锰 |
(1)上表中的“待测数据”是_____________。
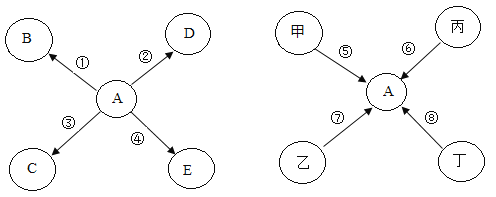
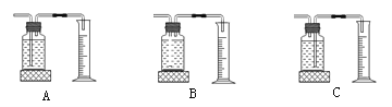
(2)如图可用于此实验收集O2的装置是_________(填字母)。一开始导管排出的气体是否收集?其理由是____________。
(3)通过实验1与实验____________的待测数据对比,可说明红砖粉能改变过氧化氢分解速率。
(4)如需证明红砖粉可作过氧化氢分解的催化剂,还需通过实验证明_______。
【题目】学习了二氧化锰对过氧化氢有催化作用的知识后。某同学想:氧化铜能否起到类似二氧化锰的催化剂作用呢?于是进行了如下探究。
(猜想)Ⅰ氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ氧化铜是反应的催化剂,反应前后_______________和_____________不变。
(实验)用天平称量![]() 氧化铜,取
氧化铜,取![]() 的过氧化氢溶液于试管中,进行如下实验:
的过氧化氢溶液于试管中,进行如下实验:
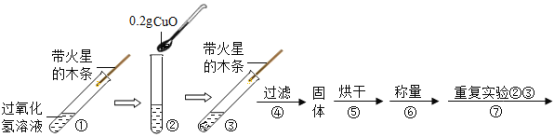
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
①_____________ ②带火星的木条复燃 | 所得固体_________g | 溶液中有气泡放出 ②带火星的木条______(填“复燃”或“不复燃”) | 猜想Ⅰ、Ⅱ不成立猜想Ⅲ成立 |
(2)步骤①的目的是___________________。
(3)过氧化氢能被氧化铜催化分解放出氧气的化学反应的文字表达式为:___________________。
(4)过氧化氢反应生成氧气的快慢除了与是否使用催化剂有关,与催化剂的种类有关外,还与什么因素有关呢?请写出你的猜想并设计实验方案验证你的猜想。
①你的猜想是过氧化氢反应生成氧气的快慢与_________________有关;
②你的实验方案是:____________________。