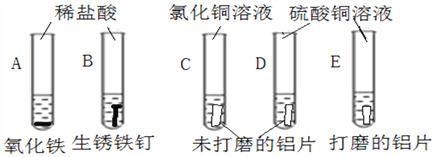
题目内容
【题目】氨气是一种无色有刺激性气味的气体,密度比空气_____,是氮肥工业的重要原料。
(1)实验室常用浓氨水和氢氧化钠固体混合制取少量氨气,产生氨气的原因有:
①氢氧化钠固体溶于水放热,促使氨水分解生成氨气,化学方程式为:_____![]() NH3↑+H2O。
NH3↑+H2O。
②氢氧化钠固体溶于水放热,使氨气在水中的_____,有利于氨气逸出。
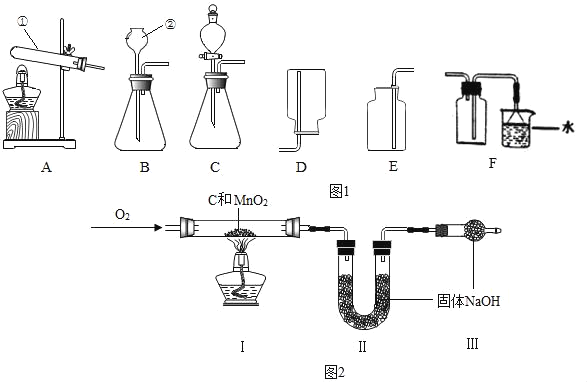
(2)某化学兴趣小组为探究分子的运动情况,在玻璃管两端同时放入蘸有溶液的棉花,做了图1所示实验,发现在玻璃管内形成了白色烟环(成分为氯化铵)且偏向蘸有浓盐酸的棉花一端。
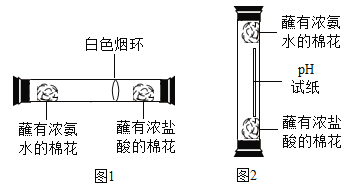
①白色烟环偏向蘸有浓盐酸的棉花一端的原因是_____;
②写出该反应的化学方程式:_____。
(3)为了获得更好的视觉效果,该小组同学设计了图2所示实验。
(实验步骤)从玻璃管顶部将蘸有浓盐酸的棉花投入底部(过程中棉花不接触管壁),pH试纸迅速变为红色;再将蘸有浓氨水的棉花固定在玻璃管顶部,用摄像机记录实验现象。
(查阅资料)图3所示是本实验所用的pH试纸的显色范围。

(现象分析)图4所示是摄像机记录下来的pH试纸每15s的显色情况。
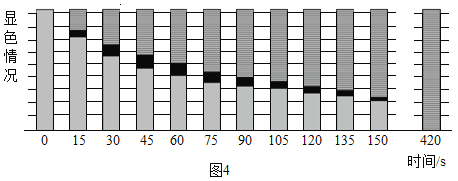
420s时,pH试纸全部变为绿色,白烟大部分沉降至量筒底部。图4中,75s时pH试纸从上至下的颜色依次为绿色、_____和_____。
(拓展探究)上述实验中,若上下棉花颠倒,即玻璃管底部是蘸有浓氨水的棉花,顶部是蘸有浓盐酸的棉花,则pH试纸几乎直接变为绿色,玻璃管内迅速充满白烟,解释产生这种现象的原因:_____。
(4)氯化铵是一种常见的氮肥。某氯化铵化肥的含氮量经测定是25.2%,已知杂质不含氮元素,则此化肥中氯化铵的质量分数为_____(计算结果保留一位小数)。
【答案】小 NH3H2O![]() H2O+NH3↑ 溶解度减小 相同条件下,氨分子比氯化氢分子运动的快 NH3+HCl═NH4Cl 黄色 红色 氯化氢气体的密度比空气大,氨气的密度比空气小,两种气体更快反应 96.3%
H2O+NH3↑ 溶解度减小 相同条件下,氨分子比氯化氢分子运动的快 NH3+HCl═NH4Cl 黄色 红色 氯化氢气体的密度比空气大,氨气的密度比空气小,两种气体更快反应 96.3%
【解析】
解:氨气是一种无色有刺激性气味的气体,密度比空气小,是氮肥工业的重要原料;
(1)①氢氧化钠固体溶于水放热,促使氨水分解生成氨气,即氨水在受热的条件下生成氨气和水;②氢氧化钠固体溶于水放热,使氨气在水中的溶解度减小,有利于氨气逸出;
(2))①相对分子质量越大,分子的运动速率越慢,相对分子质量越小,分子的运动速率越快,氨气的相对分子质量小于氯化氢的相对分子质量,所以氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端;
②氨气和氯化氢气体反应生成氯化铵,反应的化学方程式为:NH3+HCl═NH4Cl;
(3)420s时,pH试纸全部变为绿色,白烟大部分沉降至量筒底部。图4中,75s时pH试纸从上至下的颜色依次为绿色、黄色和红色;拓展探究中,产生这种现象的原因:氯化氢气体的密度比空气大,氨气的密度比空气小,两种气体更快反应;
(4)25.2%÷![]() ×100%=96.3%。
×100%=96.3%。

【题目】溶液与人们的生活息息相关。
(1)下列少量物质分别放入水中,充分搅拌,可以得到溶液的是_____(填字母)。
A 高锰酸钾 B 汽油 C 面粉 D 碘单质
(2)氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示
氢氧化钠 | 碳酸钠 | ||||
20℃ | 40℃ | 20℃ | 40℃ | ||
水 | 109g | 129g | 21.8g | 49g | |
酒精 | 17.3g | 40g | 不溶 | 不溶 | |

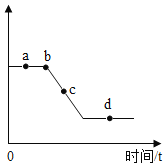
①上述图象表示_____(填“氢氧化钠”或“碳酸钠”)的溶解度曲线。
②20℃时,氢氧化钠的溶解度_____(填“大于”或“小于”)碳酸钠的溶解度。
③40℃时,分别将50gNaOH分别投入到100g水和100g酒精中,能形成饱和溶液的是_____(选填“水”或“酒精”),再将适量CO2通入所得NaOH的酒精溶液中,观察到的现象为_____,反应的化学方程式为:_____。