题目内容
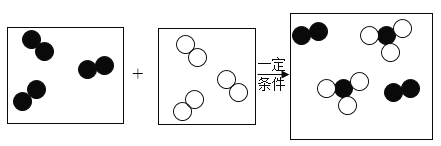
【题目】某化工厂用氢气和过量的氮气在一定条件下合成氨气(NH3),其微观过程如图所示。下列关于合成氨气的说法正确的是
A.反应后生成了两种物质
B.反应前后氮元素和氢元素的化合价均没有改变
C.参加反应的氢气和氮气的分子个数比为3:1
D.反应前后分子和原子的种类和个数均没有变化
【答案】C
【解析】
根据图示可知,氢气和过量的氮气在一定条件下合成氨气(NH3),化学方程式为N2+3H2 2NH3。
2NH3。
A、化学反应前后减少的是反成物,增加的是生应物,由微观示意图可知反应后增加了一种微粒,生成物一种,A错。
B、反应物是氮气和氢气,它们属于单质,其中氮元素和氢元素的化合价均为零价,反应后氮元素氢元素,化合价分别为-3价和+1价,化合价发生了变化,B错。
C、由分析知化学方程式为N2+3H2 2NH3,故参加反应的氢气和氮气的分子个数比为3:1,C正确。
2NH3,故参加反应的氢气和氮气的分子个数比为3:1,C正确。
D、反应前后原子的种类和个数均没有变化,分子的种类个数发生了变化,D错。
故选:C。

练习册系列答案
相关题目
【题目】金属涂层光纤是在光纤的表面徐布Cu- A1合金层的光纤。为测定金属涂层光纤材料Cu- A1合金中铝的质量分数,甲、乙、丙同学称取该样品于烧杯中,进行实验,充分反应,测得实验数据如下表:
实验 | 甲 | 乙 | 丙 |
加入合金样品粉末的质量/g | 20 | 20 | 40 |
加入稀硫酸的质量/g | 200 | 100 | 100 |
烧杯中剩余物的质量/g | 218 | 118 | 138 |
(1)实验中合金样品粉末与稀硫酸恰好完全反应的实验是 (填“甲”、“乙”或“丙”)。
(2)该铝合金中铝的质量分数为多少? (写出计算过程)
(3)实验后,甲、乙、丙同学将各自的烧杯中剩余物倒入指定容器中,指定容器中物质的总质量最终为 g。