题目内容
【题目】写出下列化学反应方程式
(1)高温煅烧石灰石_____。
(2)稀硫酸与铁锈反应_____。
(3)铜和硝酸银溶液_____。
(4)硫酸铵和氢氧化钠溶液混合共热_____。
(5)小苏打中加入稀盐酸_____。
【答案】CaCO3![]() CaO+CO2↑ Fe2O3+3H2SO4═Fe2(SO4)3+3H2O Cu+2AgNO3=2Ag+Cu(NO3)2 (NH4)2SO4+2NaOH
CaO+CO2↑ Fe2O3+3H2SO4═Fe2(SO4)3+3H2O Cu+2AgNO3=2Ag+Cu(NO3)2 (NH4)2SO4+2NaOH![]() Na2SO4+2H2O+2NH3↑ NaHCO3+HCl=NaCl+H2O+CO2↑
Na2SO4+2H2O+2NH3↑ NaHCO3+HCl=NaCl+H2O+CO2↑
【解析】
首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可。
(1)石灰石的主要成分是碳酸钙,在高温的条件下,碳酸钙分解为氧化钙和二氧化碳;故填:CaCO3![]() CaO+CO2↑
CaO+CO2↑
(2)铁锈的主要成分是氧化铁,氧化铁能与稀硫酸反应生成硫酸铁和水,故填:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
(3)铜与硝酸银反应生成银和硝酸铜;故填:Cu+2AgNO3=2Ag+Cu(NO3)2
(4)硫酸铵与氢氧化钠反应生成硫酸钠、水和氨气;故填:(NH4)2SO4+2NaOH![]() Na2SO4+2H2O+2NH3↑
Na2SO4+2H2O+2NH3↑
(5)小苏打是碳酸氢钠的俗称,碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳;故填:NaHCO3+HCl=NaCl+H2O+CO2↑

【题目】大黄同学喝“养乐多”时感觉有酸味,他猜测其中有酸。査阅资料大黄同学得知,养乐多含有乳酸。
(提出问题)乳酸是否具有酸的通性?
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
在乳酸溶液中加入石蕊 | 石蕊变红 | 乳酸具有酸的通性 |
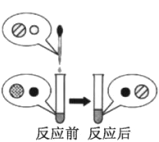
在乳酸溶液中加入_____(填化学式) | 有气泡产生,点燃气泡产生爆鸣声 | |
在乳酸溶液中加入碳酸氢钠 | _____ |
(实验反思)(1)从微粒角度看,乳酸具有酸的通性是因为其溶液中存在大量_____;
(2)乳酸化学符号用HL表示,写出乳酸和碳酸氢钠反应的化学方程式_____。
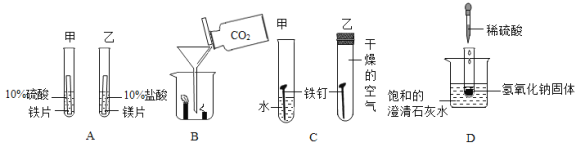
(定量研究)为测定乳酸组成元素和化学式,称取6.0g乳酸放入如图加热装置中(夹持仪器未画出),通入充足氧气使之完全燃烧,将反应后的混合气体先后通过装置B、C.试回答:

(1)为顺利完成实验,将方框内所示装置放入B、C位置时,正确的导管连接顺序是:_____→_____→_____→_____;
(2)按正确方式连接B、C装置进行实验,实验后测得氢氧化钠溶液增重_____g,浓硫酸增重3.6g,则乳酸中碳元素:氢元素质量比=6:1;
(3)已知乳酸相对分子质量是90,则乳酸的化学式为_____。
(反思拓展)乳酸经过聚合反应可以制成聚乳酸塑料[(C3H4O2)n,n>1000],聚乳酸塑料常温下会降解生成CO2和H2O.以下对聚乳酸认识正确的是_____。
A 聚乳酸制成的外卖快餐饭盒,不会产生“白色污染”
B 聚乳酸是一种有机高分子化合物
C 聚乳酸降解发生了分解反应
D聚乳酸中碳元素:氢元素:氧元素质量比=9:1:8