题目内容
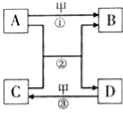
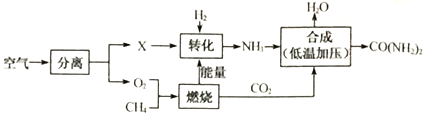
【题目】某化工厂用废硫酸制备硫酸钾的流程如下,请回答下列问题:

资料:己知20℃时硫酸铵、硫酸钾溶解度如下表:
物质 | 硫酸钾 | 氯化钾 | 氯化铵 | 硫酸铵 |
溶解度/g(20℃) | 11.1 | 34.2 | 37.2 | 75.4 |
(1)“设备I”中将碳酸钙研成粉末的目的是_____。
(2)“设备II”中发生的化学反应方程式是_____。
(3)“设备III”中发生的化学反应方程式是_____。反应物之一硫酸铵[(NH4)2SO4)]中氮元素的化合价为_____。洗涤从“设备III”中得到的固体时,不用水而是用饱和硫酸钾溶液,其目的是_____。
(4)上述流程中可循环使用的物质除水外,还有_____(填写化学式).
(5)根据本题所给的信息推断实验室_____(能、不能)用碳酸钙粉末和稀硫酸反应制备得到二氧化碳。
【答案】增大反应物接触面积,加快反应速率,使反应更充分 CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH4)2SO4 (NH4)2SO4+2KCl=2NH4Cl+K2SO4↓ -3 减少硫酸钾的溶解 CaCO3、NH3 能
【解析】
(1)碳酸钙研成粉末的目的是增大反应物接触面积,加快反应速率,使反应更充分;
(2)根据流程图可知,“设备Ⅱ”中反应物是硫酸钙、氨气、二氧化碳和水,生成物是碳酸钙和硫酸铵,反应的方程式是:CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH4)2SO4;
(3)根据流程图可知,“设备III”中反应物是硫酸铵和氯化钾,生成物是氯化铵和硫酸钾,此时由于硫酸钾的溶解度较小而析出,形成沉淀,反应的化学反应方程式是(NH4)2SO4+2KCl=2NH4Cl+K2SO4↓;根据化合物中各元素化合价的代数和为零可知,在(NH4)2SO4)中,由于硫酸根显-2价,可推出铵根显+1价,由于氢显+1价,可推出氮元素显-3价;饱和硫酸钾溶液不能溶解硫酸钾,能溶解其他物质。洗涤从“设备Ⅲ”中得到的固体时,不用水而是用饱和硫酸钾溶液,其目的是减少硫酸钾的溶解;
(4)根据在前面反应物中有,到了后面生成物中有,这样的物质可以循环使用,所以由图示可知CaCO3、NH3可以循环使用;
(5)根据本题所给的信息推断实验室能用碳酸钙粉末和稀硫酸反应制备得到二氧化碳。

 智慧小复习系列答案
智慧小复习系列答案【题目】为了测定某地石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行如下实验:(请写出详细的计算过程)
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(g) | 5 | 10 | 15 | 20 |
生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | 4.4 |
(1)计算这种石灰石样品中碳酸钙的质量分数___.
(2)计算出实验所用稀盐酸中HCl的质量分数___.
【题目】为探究CO2与NaOH溶液发生的反应,某兴趣小组尝试用不同的方式进行实验。
(查阅资料)
20℃时,几种物质在水中的溶解度见表:
物质 | Na2CO3 | NaHCO3 | Ca(OH)2 | Ba(OH)2 |
溶解度/g | 21.5 | 9.6 | 0.165 | 3.89 |
(实验探究)
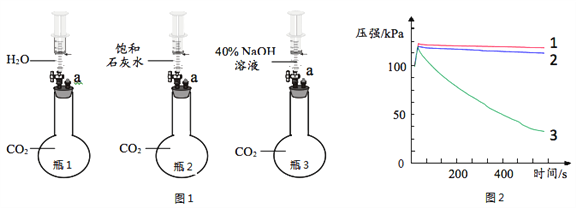
(1)实验一:小雨取一充满CO2的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪,小雨另取一相同的充满CO2的矿泉水瓶,向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时观察到的现象是_____。
(2)实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液X少许,向其中滴加BaCl2溶液,有白色沉淀产生,该反应的化学方程式为_____。实验中不宜将BaCl2溶液换成CaCl2溶液的原因是_____。
(3)实验三:小华取实验一所得溶液X少许,向其中加入过量的BaCl2溶液,振荡,静置,取上层清液,滴入1滴酚酞试液,发现溶液呈_____色,证明溶液X中有NaOH剩余。实验中,小华没有直接向少量溶液X中滴入酚酞试液,理由是_____。
(4)实验四:兴趣小组将CO2持续通入一定浓度一定量的NaOH溶液中,用数字化实验技术测定反应过程中温度变化,结果如图所示。图中,AB段温度变化的原因是_____。

(反思感悟)
(5)实验从CO2减少、NaOH减少、Na2CO3生成等物质的变化,以及_____转化等视角多维度探究CO2与NaOH发生了反应,对于现象不明显的化学反应,可以通过现代技术手段进行数据测定,实现反应过程的“可视化”。