题目内容
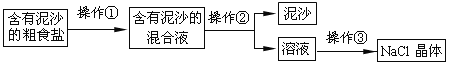
【题目】某固体粉末可能含有碳酸钙、氧化铜、氧化铁、木炭粉中的几种,取mg该固体粉末按下列流程进行实验(本流程涉及到的反应均为初中化学常见的反应,且各步均恰好完全反应)。
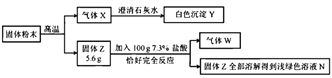
下列说法中正确的是
A. 溶液N中只含一种溶质
B. 原固体粉末中可能含有碳酸钙
C. 白色沉淀Y一定是碳酸钙,气体W一定是氢气
D. 原固体粉末中一定没有氧化铜,一定含有碳酸钙
【答案】BC
【解析】
能使澄清石灰水变浑浊的气体是二氧化碳,所以X是CO2,二氧化碳与澄清石灰水反应生成碳酸钙,Y是CaCO3;N是浅绿色溶液,N中含有Fe2+,固体粉末中含有氧化铁、木炭粉,3C+2Fe2O3 ![]() 4Fe+3CO2↑,Fe +2HCl== FeCl2+H2↑,所以w是氢气。则固体粉末中一定含有氧化铁、木炭粉,可能含有碳酸钙,因为固体Z完全溶于酸,氧化铜和碳反应生成的铜不与酸反应,故粉末中无氧化铜。A. 溶液N中含 FeCl2,CaO + 2HCl == CaCl2 + H2O,可能含CaCl2 ,错误;B. 原固体粉末中可能含有碳酸钙,正确;C. 白色沉淀Y一定是碳酸钙,气体W一定是氢气,正确;D. 氧化铜和碳反应生成的铜不与酸反应,固体Z完全溶于酸,所以原固体粉末中一定没有氧化铜,可能含有碳酸钙,错误。故选BC。
4Fe+3CO2↑,Fe +2HCl== FeCl2+H2↑,所以w是氢气。则固体粉末中一定含有氧化铁、木炭粉,可能含有碳酸钙,因为固体Z完全溶于酸,氧化铜和碳反应生成的铜不与酸反应,故粉末中无氧化铜。A. 溶液N中含 FeCl2,CaO + 2HCl == CaCl2 + H2O,可能含CaCl2 ,错误;B. 原固体粉末中可能含有碳酸钙,正确;C. 白色沉淀Y一定是碳酸钙,气体W一定是氢气,正确;D. 氧化铜和碳反应生成的铜不与酸反应,固体Z完全溶于酸,所以原固体粉末中一定没有氧化铜,可能含有碳酸钙,错误。故选BC。

【题目】某化工厂用废硫酸制备硫酸钾的流程如下,请回答下列问题:
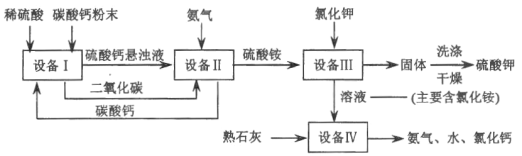
资料:己知20℃时硫酸铵、硫酸钾溶解度如下表:
物质 | 硫酸钾 | 氯化钾 | 氯化铵 | 硫酸铵 |
溶解度/g(20℃) | 11.1 | 34.2 | 37.2 | 75.4 |
(1)“设备I”中将碳酸钙研成粉末的目的是_____。
(2)“设备II”中发生的化学反应方程式是_____。
(3)“设备III”中发生的化学反应方程式是_____。反应物之一硫酸铵[(NH4)2SO4)]中氮元素的化合价为_____。洗涤从“设备III”中得到的固体时,不用水而是用饱和硫酸钾溶液,其目的是_____。
(4)上述流程中可循环使用的物质除水外,还有_____(填写化学式).
(5)根据本题所给的信息推断实验室_____(能、不能)用碳酸钙粉末和稀硫酸反应制备得到二氧化碳。