��Ŀ����
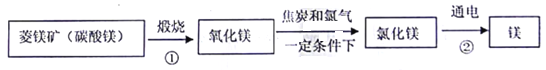
����Ŀ�������DZ������Ȼ��Դ����ͼ���Կ�����Ϊԭ�Ϻϳ�����[CO(NH2)2]�����̡��밴Ҫ��ش��������:

(1)��������__________(�����������������������)��X�ǿ����к����������壬�����ʽΪ________________��
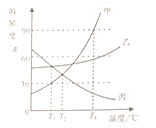
(2)ͼ�з�������Ĺ�������________�仯(����������������ѧ��)��
(3)�����к��е�����ϡ������Ļ�ѧ����_________(���������������ȶ���)��
(4)ʵ�����ô���ʯ��ϡ������ȡ������̼�Ļ�ѧ��Ӧ����ʽΪ_____________��������̼���ܶȱȿ���__________(������������С��)��
(5)����Ȼ������Ҫ�ɷ���CH4����Ȼ������__________������Դ(������������������)��
�ڵ�ȼCH4֮ǰӦ__________�� 8g CH4��ȫȼ������32gO2������agCO2��18gH2O����a=__________��
����CH4�ڸ������е����ñ�������ѧ��Ӧ�з������ʱ仯��ͬʱҲ�������________�仯(��������������ԭ�Ӹ�����)��
(6)��������_______(�����������������������ط���)��д��NH3�ϳ����صĻ�ѧ��Ӧ����ʽ_____________��
���𰸡� ����� N2 ���� �ȶ� CaCO3+2HCl�TCaCl2+H2O+CO2�� �� ���� �������Ĵ��� 22 g ���� ���� CO2+2NH3![]() CO(NH2)2+H2O
CO(NH2)2+H2O
��������������Ҫ�����˴�����ͻ������б𣬳������ʵ���������ã���ѧ�仯�������仯���б������غ㶨�ɵ�Ӧ�ã���ѧ����ʽ����д�ȡ����ʱҪ���ݸ������ʵ����ʣ���ϸ������������з������жϵó���ȷ�Ľ���
��1�������к��ж��ֳɷ֣����ڻ���X�ǿ����к����������壬�������ǵ����������ʽΪN2��
��2��ͼ�з�������Ĺ���û�����������ʣ����������仯��
��3�������к��е�����ϡ������Ļ�ѧ�����ȶ���
��4��ʵ�����ô���ʯ����ʯ��ʯ����ϡ������ȡ������̼������ʯ����ʯ��ʯ������Ҫ�ɷ���̼��ƣ�̼��ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼����ѧ��Ӧ����ʽΪCaCO3+2HCl�TCaCl2+H2O+CO2����������̼���ܶȱȿ�����
��5������Ȼ�����ڲ���������Դ��
�ڿ�ȼ�����岻��ʱ��ȼ����ȿ��ܲ�����ը����ȼCH4֮ǰӦ�������Ĵ��ȡ� 8g CH4��ȫȼ������32gO2������agCO2��18gH2O�����������غ㶨�ɣ���a=8g+32g��18g=22g��
�۸�������ͼ��֪����ѧ��Ӧ�з������ʱ仯��ͬʱҲ������������仯��
��6������ֻ����Ӫ��Ԫ�ص�Ԫ�أ����ڵ��ʣ���������ͼ��֪��������̼��NH3�ڵ��¸�ѹ���ܷ�Ӧ�������غ�ˮ����Ӧ��ѧ����ʽΪCO2+2NH3![]() CO(NH2)2+H2O��
CO(NH2)2+H2O��

 ��ٽ������½������������ϵ�д�
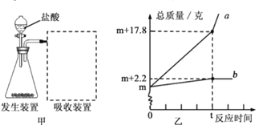
��ٽ������½������������ϵ�д�����Ŀ������һ�ֻ��ý���������������������ˮ�����ʷ�����Ӧ������ˮ��Ӧ�Ļ�ѧ����ʽΪ:2Na+2H2O==2NaOH+H2������ʵ���ң�С����ȡ����������ͭ��Һ���ձ��У���ȡһС����Ͷ������ͭ��Һ�У���ַ�Ӧ����ˣ��õ���Һ����ɫ�����������˱��ijɷֽ���̽����
�������������Һ�����ʵijɷ���ʲô?
������������Na2SO4��Һ������
�����������������һ:Na2SO4
�����:Na2SO4��NaOH
������:____________
������:Na2SO4��CuSO4��NaOH
С����Ϊ����______��������������_______(�û�ѧ����ʽ��ʾ)��
��ʵ������֤��
ʵ�� | ʵ����� | ʵ��F�� | ʵ����� |
ʵ��һ | ȡ������Һ���Թ��У���ϸ�۲����� | ��ҺΪ��ɫ | ����_____������ |
ʵ��� | ��ʵ��һ��ȡ��Һ�е����̪��Һ | ________ | ����������� |
ʵ���� | �����£���ȡ������Һ������Һ���� | pH=7 | ����_____���� |
����չ�������������˳������Ƽ�ǰ��Ľ���____(������������������)��λ�ں���Ľ�������������Һ���û�������