题目内容
【题目】已知:在水溶液中,乙醇(C2H5OH)不发生电离;溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br-);氢氧化钠电离产生钠离子和氢氧根离子。请回答下列问题:
(1)根据这三种溶液的组成推断,溴化氢的水溶液显_______性。
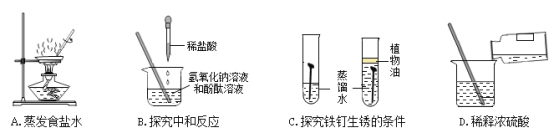
(2)写出上述物质之间发生中和反应的化学方程式____________________________。
【答案】酸 ![]()
【解析】
(1)溴化氢在水中电离出的阳离子全部是氢离子,因此水溶液显酸性,故填:酸。
(2)溴化氢在水中电离出的阳离子全部是氢离子,符合酸的组成特点,属于酸,氢氧化钠在水溶液中电离出的阴离子全部是氢氧根离子,符合碱的组成特点,属于碱,酸和碱反应生成盐和水的反应属于中和反应,溴化氢和氢氧化钠反应生成溴化钠和水,反应的化学方程式:![]() ,故填:
,故填:![]() 。
。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】下表列出了固体物质A在不同温度时的溶解度
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
(1)80℃时,向盛有100g水的烧杯中加入30g固体A,充分溶解后形成溶液的质量为_____g,再将烧杯内物质温度降至20℃,此时溶液中溶质与溶剂的质量比为_____(填最简整数比)。
(2)通过对上表数据的分析,物质A的溶解度曲线应是图中的_____(填“甲”或“乙”)。
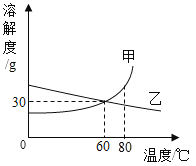
(3)80℃时,配制一定量甲物质的溶液,将其降温到60℃,是否有固体析出?_____(填“有”、“没有”或“不确定”)。