题目内容
【题目】现有硫酸钠和氯化钠的固体混合物15.0g,其中含氧元素6.4g,将该混合物加入到一定质量的氯化钡溶液中,恰好完全反应,得到199.7g氯化钠溶液,请计算:
(l)硫酸钠(Na2SO4)中硫元素和氧元素的质量比为 。
(2)15.0g固体混合物中硫酸钠的质量为 g。
(3)所用氯化钡溶液中溶质的质量分数(结果保留至0.1%)。
【答案】(l)1:2 (2)14.2 (3)10.0%
【解析】
(1)硫酸钠(Na2SO4)中硫元素和氧元素的质量比为(32×1):(16×4)=1:2,故填:1:2。
(2)硫酸钠质量:6.4g÷![]() =14.2g,故填:14.2。
=14.2g,故填:14.2。
(3)解:设15.0g的硫酸钠完全反应消耗的BaCl2的质量为x,生成硫酸钡的质量为y
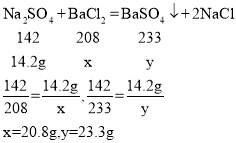
则氯化钡溶液中溶质的质量分数=![]()
答:所用氯化钡溶液中溶质的质量分数10.0%。

练习册系列答案
相关题目