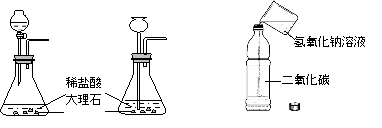题目内容
【题目】根据要求回答问题。
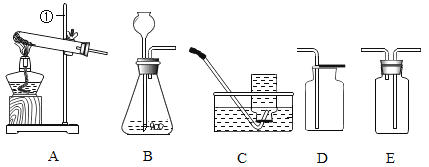
(1)写出仪器①的名称___________________。
(2)用氯酸钾和二氧化锰制取氧气的化学方程式为___________,该反应属于_____________(填基本反应类型),二氧化锰的作用是___________。 用装置C收得的氧气不纯,可能的原因是___________。
(3)实验室用稀盐酸和石灰石制取CO2,选用的发生装置是___________, 反应的化学方程式为___________。将气体通过盛有___________的E装置,可得到干燥的CO2。
(4)为验证可燃物燃烧需要氧气,某同学利用中间凹陷的软质塑料瓶设计如下实验。
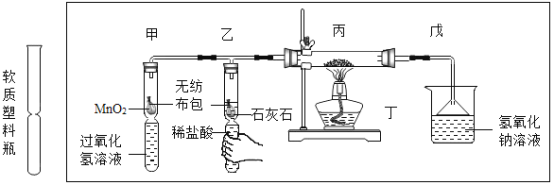
①通过捏放软塑料瓶下端可控制_______________。
②实验步骤:先捏住乙处瓶身一段时间(如图所示),后点燃丁处酒精灯,观察到丙处无明显变化;放开乙处瓶身,____________(填具体操作),丙中红磷燃烧,产生白烟。结论:燃烧需要氧气。实验中,先捏住乙处瓶身一段时间的目的是_____________。
③戊中氢氧化钠溶液可吸收有毒的五氧化二磷,生成磷酸钠(Na3PO4)和水,反应的化学方程式为_____________。
【答案】铁架台 2KClO3![]() 2KCl+3O2↑ 分解反应 催化作用 导管口一有气泡冒出就开始收集或集气瓶内留有气泡等 B CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸 反应的发生与停止 捏住甲处瓶身下半部分一段时间 排除装置的空气与后面要做的实验形成对比 6NaOH+P2O5=2Na3PO4+3H2O
2KCl+3O2↑ 分解反应 催化作用 导管口一有气泡冒出就开始收集或集气瓶内留有气泡等 B CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸 反应的发生与停止 捏住甲处瓶身下半部分一段时间 排除装置的空气与后面要做的实验形成对比 6NaOH+P2O5=2Na3PO4+3H2O
【解析】
(1)仪器①的名称:铁架台;
(2)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3![]() 2KCl+3O2↑;符合“一变多”的特点,是分解反应;在这个反应中二氧化锰起催化作用;用装置C收得的氧气不纯,可能的原因是:导管口一有气泡冒出就开始收集或集气瓶内留有气泡等;
2KCl+3O2↑;符合“一变多”的特点,是分解反应;在这个反应中二氧化锰起催化作用;用装置C收得的氧气不纯,可能的原因是:导管口一有气泡冒出就开始收集或集气瓶内留有气泡等;
(3)实验室用稀盐酸和石灰石制取CO2,不需要加热,可选用B装置作发生装置;化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳不和浓硫酸反应,可以用浓硫酸干燥二氧化碳;所以将气体通过盛有的浓硫酸E装置,可得到干燥的CO2;
(4)①根据装置的特点可知,通过捏放软塑料瓶下端可控制反应的发生与停止;
②根据控制变量实验法的方法可知,先捏住乙处瓶身一段时间(如图所示),后点燃丁处酒精灯,观察到丙处无明显变化;放开乙处瓶身,捏住甲处瓶身下半部分一段时间,丙中红磷燃烧,产生白烟;实验中,捏住乙处瓶身一段时间的目的是排除装置的空气与后面要做的实验形成对比;
③五氧化二磷和氢氧化钠反应生成磷酸钠和水,化学方程式为:6NaOH+P2O5=2Na3PO4+3H2O。
故答案为:
(1)铁架台;
(2)2KClO3![]() 2KCl+3O2↑;分解反应;催化作用;导管口一有气泡冒出就开始收集或集气瓶内留有气泡等;
2KCl+3O2↑;分解反应;催化作用;导管口一有气泡冒出就开始收集或集气瓶内留有气泡等;
(3)B;CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸;
(4)①反应的发生与停止;
②先捏住甲处瓶身下半部分一段时间;排除装置的空气与后面要做的实验形成对比;
③6NaOH+P2O5=2Na3PO4+3H2O。

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】同学们对“影响金属与盐酸反应剧烈程度的因素”进行了探究。
[提出问题]金属与盐酸反应剧烈程度受哪些因素影响?
[做出猜想] Ⅰ.与盐酸的浓度有关Ⅱ .与____________有关Ⅲ.与金属的种类有关
[进行实验]
实验编号 | 金属 | 盐酸的质量分数% | 温度℃ | 金属丝消失的时间s |
① | 铝丝 | 5 | 20 | 450 |
② | 铝丝 | 8 | 20 | t |
③ | 铝丝 | 10 | 20 | 240 |
④ | 铝丝 | 10 | 30 | 65 |
⑤ | 铁片 | 10 | 30 | 125 |
[解释与结论]
(1)补充猜想:金属与盐酸反应剧烈程度,与____________有关。
(2)铝与盐酸反应的方程式为_________________。
(3)由实验①③可知,猜想1___________。(填“成立”或“不成立”)。在实验②中,铝丝消失的时间(用t表示)的取值范围是_________________。
(4)有同学认为通过实验④⑤并不能证明“猜想与假设Ⅲ”成立,理由是_________________。
【题目】牙膏是一种日用必需品。某兴趣小组对某一品牌牙膏中所含摩擦剂的成分进行了如下探究。
[查阅资料]
(1)常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2。
(2)牙膏中除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体。
(3)SiO2不溶于水,也不与盐酸反应。氢氧化铝和稀盐酸可以发生中和反应。
(4)AI(OH)3能和氢氧化钠溶液发生反应,该反应的化学方程式为:Al(OH)3+NaOH=NaAlO2+2_____(填化学式)
[提出问题]:该品牌牙膏的酸碱性如何?其中含有什么摩擦剂?
[实验与猜想]
(1)取少量牙膏膏体于小烧杯中,加入10毫升蒸馏水,充分搅拌,静置一段时间,分离上层清液和沉淀;
(2)用____(填字母)测定所得溶液的pH值大于7。
A pH试纸
B 紫色石蕊试液
C 酚酞试液
(3)取少量沉淀物加入过量的稀盐酸,沉淀物全部溶解并有大量气泡产生,同时得到澄清溶液,如图所示,则该品牌牙膏中一定含有碳酸钙,一定不含有_____。
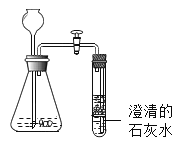
(4)进行猜想:摩擦剂成分可能是a.只含碳酸钙b._____。
[设计实验]同学们为进一步 确认摩擦剂中含有氢氧化铝,进行了如下实验:
实验步骤 | 实验现象 | 解释与结论 |
取实验(3)中锥形瓶内反应后的澄清溶液,逐滴滴入定量氢氧化钠溶液 | 开始无明显现象,后产生大量白色沉淀 | 开始无明显现象,是因为开始时加入的氢氧化钠溶液和过量的____反应。继续滴入氢氧化钠化钠溶液后产生白色沉淀原因是_____(用化学方程式表示) |
继续滴入氢氧化钠溶液至过量 | 白色沉淀溶解 | 摩擦剂中还含有氢氧化铝 |
[实验结论]该牙膏摩擦剂成分可以确定。
[总结与提升]判断混合物中物质成分时,除了要考虑生成物,还要考虑_____。