题目内容
【题目】根据下列装置,回答问题。
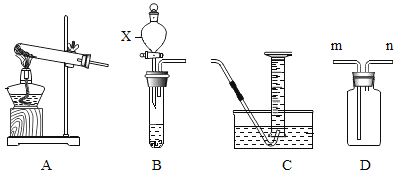
(1)写出装置图中标号仪器的名称:x_____。
(2)甲兴趣小组用上述装置测定KClO3和MnO2混合粉末中KClO3的质量分数。
①选用的发生装置是_____(填字母)。
②KClO3和MnO2发生反应的化学方程式为_____,反应的基本类型为_____反应
③装置D装满水,也可用于排水法收集O2,则O2应从导管_____(填“m”或“n”)通入。
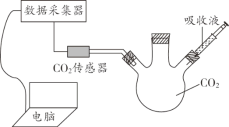
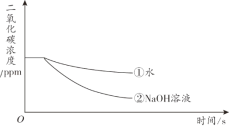
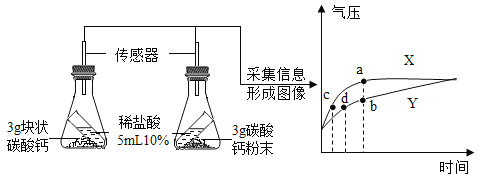
(3)乙兴趣小组利用下图数字化实验可以形象地比较块状和粉末状碳酸钙与稀盐酸反应的速率,反应发生后,锥形瓶内气压的变化如曲线所示。
①锥形瓶中发生反应的化学方程式为_____。
②曲线_____(填“X”或“Y”)表示块状碳酸钙与稀盐酸反应。
③点_____(填“a”、“b”、“c”或“d”)表示碳酸钙与盐酸反应已停止。
④两个锥形瓶中都完全反应结束后,两者产生的二氧化碳,_____(填字母)。
A 粉末状碳酸钙多
B 块状碳酸钙多
C 一样多
【答案】分液漏斗 A ![]() 分解 n
分解 n ![]() Y a C
Y a C
【解析】
(1)装置图中标号仪器的名称:x分液漏斗;
(2)①氯酸钾在二氧化锰的作用下受热分解生成氯化钾和氧气,选用的发生装置是固-固加热型A;
②KClO3在MnO2催化作用下,加热条件下分解生成氯化钾和氧气,发生反应的化学方程式为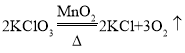 ,反应的特点是一变多,基本类型为分解反应;
,反应的特点是一变多,基本类型为分解反应;
③氧气的密度小于水,装置D装满水,也可用于排水法收集O2,则O2应从导管n通入;
(3)①锥形瓶中发生反应是碳酸钙和盐酸生成二氧化碳、氯化钙和水,化学方程式为![]() ;
;
②反应物间接触越充分,反应越快,块状碳酸钙与盐酸反应的速率小于粉状碳酸钙,曲线Y表示块状碳酸钙与稀盐酸反应;
③点a气压不再改变,说明反应结束,已经不再生成气体,表示碳酸钙与盐酸反应已停止;
④反应物颗粒的大小只影响反应物的接触程度,影响反应速率,不影响生成物的质量,两个锥形瓶中都完全反应结束后,两者产生的二氧化碳一样多。故选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】氯气(Cl2)是黄绿色气体,氯气溶于水部分以Cl2分子存在于溶液中,部分与水反应![]() ,产物中,次氯酸HClO是一种弱酸。氯气溶于水所得溶液称为氯水。把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色。如图是实验室制取氯气的成套装置图,请填空:
,产物中,次氯酸HClO是一种弱酸。氯气溶于水所得溶液称为氯水。把品红试纸(染有品红颜料的滤纸)放入氯水中,品红试纸褪色。如图是实验室制取氯气的成套装置图,请填空:
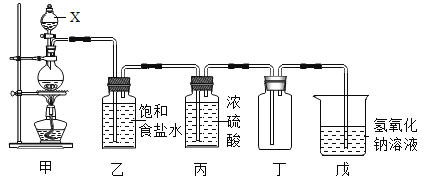
(1)仪器X的名称是:__________________。
(2)在装置丁中收集氯气,其收集方法为__________________。
(3)晓红对“氯水使品红试纸褪色”产生兴趣,她所在的学习小组进行了如下探究,请你一起来完成:
[提出问题]氯水中的什么成分使品红试纸褪色?
[猜想]猜想1:氯水中的水使品红试纸褪色;
猜想2:氯水中的Cl2使品红试纸褪色;
猜想3:氯水中的盐酸使品红试纸褪色;
猜想4:氯水中的________________(填化学式)使品红试纸褪色。
[实验探究]
实验操作 | 实验现象 | 结论 |
① 把品红试纸放入水中 | ______________ | 猜想1不成立 |
②把品红试纸放入干燥的氯气中 | 试纸不褪色 | 猜想2不成立 |
③_________________________ | 试纸不褪色 | 猜想3不成立 |
[结论]学习小组通过讨论,找到了氯水中使品红试纸褪色的物质。
[反思]向氯水中滴加几滴紫色石蕊试液,会观察到的现象是__________________。