题目内容
【题目】(1)下图是利用海水提取粗盐的过程:
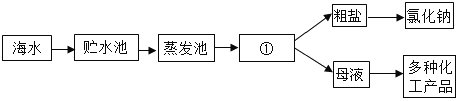
上图中①是_________池(填“结晶”或“冷却”)。
(2)粗盐中含有少量 CaCl2、MgCl2、Na2SO4 和泥沙,某同学将该粗盐样品进行提纯。
①将样品加适量水溶解,然后进行_____________,除去泥沙等难溶性杂质,得到澄清溶液。
②向所得的澄清溶液中依次加入稍过量的BaCl2 溶液、NaOH 溶液和___________(填化学式)溶液,除去生成的沉淀后,再滴加稍过量的稀盐酸,得到较纯净的NaCl 溶液。
③蒸发溶液时,当蒸发皿中出现___________时,停止加热,利用余热蒸干滤液。
【答案】结晶 过滤 Na2CO3 较多固体
【解析】
(1)氯化钠的溶解度受温度影响变化不大,可用蒸发结晶的方法进行分离,所以图①中是结晶池;
(2)①将样品加适量水溶解,然后进行过滤,除去泥沙等难溶性杂质,得到澄清溶液;
②向所得的澄清溶液中依次加入稍过量的BaCl2溶液(除去硫酸钠)、NaOH溶液(除去氯化镁)和Na2CO3溶液(除去氯化钙和过量的氯化钡),除去生成的沉淀后,再滴加稍过量的稀盐酸,得到较纯净的NaCl溶液;
③蒸发溶液时,当蒸发皿中出现较多固体时,停止加热,利用余热蒸干滤液。

【题目】某兴趣小组的同学从超市购买一袋食盐,欲检测其是否为加碘食盐(加碘食盐中的碘元素以碘酸钾的形式存在,碘酸钾的化学式为(KIO3)。他们査阅资料得知,加碘食盐中的KIO3在酸性条件下能与KI溶液发生反应,生成碘(I2),淀粉遇I2变蓝色。
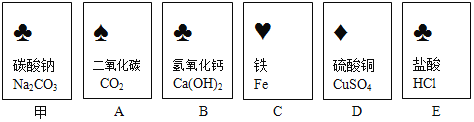
现提供下列试剂和生活中常见的物质:
(1)现有下列试剂和常见的物质:①KI溶液②纯碱③米汤④白糖⑤白酒⑥白醋,该小组同学进行实验必须选用的试剂和物质是(___________)(填字母)。
A ①③④ B ①③⑥ C ②④⑥ D ①④⑤
(2)实验确定这袋食盐是加碘食盐,他们仔细阅读包装袋上的说明后,提出问题并继续探究。
问题一:食盐是比较稳定的,而说明中强调“防热”,是否因为受热会造成碘的损失?
(实验一)探究温度对碘损失率的影响
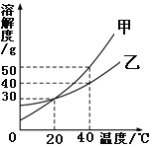
老师指导他们将一定浓度的碘酸钾溶液分成等份,在不同温度下加热十分钟后,用硫代硫酸钠标准溶液测定碘酸钾溶液的浓度,计算碘损失率并记录如表:
温度 | 30 | 50 | 80 | 100 |
碘损失率(%) | 0 | 30% | 67% | 100% |
分析上表可得出的结论是____。
(3)若要控制碘的损失率在50%左右,做菜时最好将温度范围控制在(___________)
A 0![]() ~30
~30![]() B 30
B 30![]() ~50
~50![]() C 50
C 50![]() ~80
~80![]() D 80
D 80![]() ~100
~100![]()
(4)探究酸碱度对碘损失率的影响:
①此组对照实验,需控制在碘酸钾溶液的浓度和质量、加热的___均相同,溶液的酸碱度不同的条件下进行。
②实验需要调节溶液的酸碱性,下列物质不能选用的是(___________)
A 纯碱粉末 B 食盐晶体 C 食醋
【题目】皮蛋是一种我国传统美食。它是将鸭蛋浸入一种特制的料液中,再加工而成。根据题意回答 有关问题。
[查阅资料] 将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后即得到料液。
[提出问题] 料液中除含有 NaOH 和 NaCl 外,还含有那些溶质?
[作出猜想]
(1)甲:只有Ca(OH)2;乙:_______________;丙:既有Ca(OH)2,也有Na2CO3。上述猜想中,肯定错误的是____________,其他两个还需探究。
[实验探究]
方案一 为了验证猜想,陈同学设计了如下实验:
实验步骤 | 实验现象 | 结论 |
取少量滤液,滴加酚酞试剂 | 溶液变红 | 甲 |
(2)您认为陈同学____________(是或否)能验证猜想,说出你的理由______________。
(3)方案二 为了验证猜想,李同学提出设计如下实验:
实验步骤 | 实验现象 | 结论 |
①取少量上层料液过滤,取滤液滴加足量稀盐酸 | 无明显现象 | _______正确(填甲或乙或丙) |
②另取少量滤液,滴加碳酸钠溶液 | 有白色沉淀生成 ,写出化学方程式 _______________ |
[问题与思考]
(4)实验①加入足量稀盐酸的目的是__________________。
(5)皮蛋食用时加入一些食醋,可以去除涩感,原因是:_______________ 。