题目内容
【题目】2018年10月24日上午,被称为“现代世界新七大奇迹”之一的港珠澳大桥正式通车运营。
(1)大桥建设过程中离不开吊装,吊装缆绳采用的超高分子聚乙烯纤维干法纺丝。聚乙烯的化学式为(C2H4)n,其中碳、氢元素的质量比为_____。
(2)大桥横跨“伶仃洋”。海洋中蕴含丰富的水资源,海水属于_____(填“纯净物”或“混合物”),我们可以通过_____操作除去海水中的难溶性杂质。检验海水是硬水还是软水的方法是_____。

【答案】6:1 混合物; 过滤; 向海水中加入适量的肥皂水,搅拌,若产生大量泡沫则为软水,若产生的泡沫较少则是硬水
【解析】
(1)聚乙烯的化学式为(C2H4)n,其中碳、氢元素的质量比为(12×2n):(1×4n)=6:1;
(2)海水是由多种物质组成的,属于混合物;过滤可以除去海水中的难溶性杂质,检验硬水与软水常用肥皂水,向海水中加入适量的肥皂水,搅拌,若产生大量泡沫则为软水,产生的泡沫较少的是硬水。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某研究小组用如图所示装置,探究能否用镁条代替红磷测定空气中氧气含量。

(提出猜想)
猜想1:可以代替,因为镁条与氧气反应后不会产生气体
猜想2:不能代替,因为镁条可能会与空气中的其他成分发生反应
(进行实验)
步骤 | 实验操作 | 实验现象 |
Ⅰ | 组装好装置后,打开止水夹,手捂集气瓶,一段时间后,松开手 | 烧杯中导管口有气泡冒出,松手后,烧杯中导管末端有一段液柱 |
Ⅱ | 关闭止水夹,点燃镁条,迅速伸入集气瓶中,塞好塞子 | 镁条燃烧,放出大量热,发出耀眼白光,生成大量白烟,剩余固体为白色带状物还夹杂着极少量淡黄色的固体 |
Ⅲ | 冷却至室温,打开止水夹 | 烧杯中水从导管进入集气瓶中,体积约为集气瓶体积的 |
(解释与结论)
(1)步骤Ⅰ的实验目的是_____。
(2)步骤Ⅱ中,关闭止水夹的目的是_____。
(3)根据实验现象中的_____(写一个即可)可以推测猜想2成立。
①(继续探究)经查阅资料得知氮化镁(Mg3N2)为淡黄色的固体,于是小晴猜想镁条还可能会与空气中的_____发生反应;
②(设计实验)她设计实验方案证明自己的猜想_____;
③(实验结论)镁条与氮气反应的化学方程式为:_____;
④(反思与评价)通过上述探究活动,你对燃烧有什么新的认识?_____。
【题目】回答下列问题:
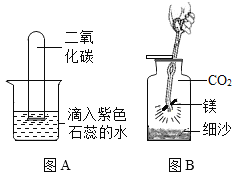
(1)如图A所示,将充满CO2的试管倒扣在滴有石蕊溶液的蒸馏水中,观察一段时间,请将观察到的现象,以及对该现象的解释填入下表:
实验现象 | 解释 |
①_____ | _____ |
②_____ | _____ |
(2)如图B所示,将镁条点燃后迅速伸入盛满CO2的集气瓶中,镁条在CO2中剧烈燃烧反应的化学方程式为:2Mg+CO2![]() 2MgO+C,请推测镁条在CO2中燃烧的现象:剧烈燃烧,________________________________ 。
2MgO+C,请推测镁条在CO2中燃烧的现象:剧烈燃烧,________________________________ 。