题目内容
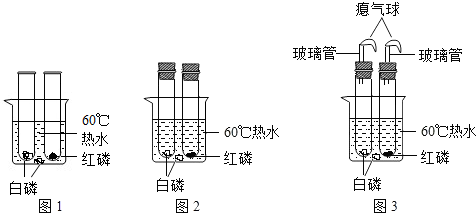
(8分)为了探究燃烧的条件,某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究。探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,……燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3)。
【变流与讨论】白烟对人体健康有害,该实验装置必须改进。
【改进与实验】同学们按改进后的图2装置进行实验。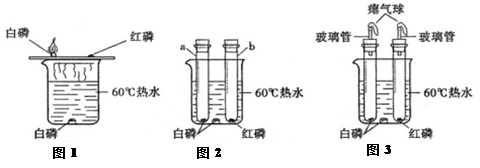
请你帮助他们将下表补充完整。
| 现 象 | 解 释 |
| a试管中白磷燃烧,热水中白磷没有燃烧。 b试管中红磷没有燃烧。 | ①a试管中白磷燃烧的化学方程式是 : ; ②热水中白磷没有燃烧的原因是: ; ③b试管中红磷没有燃烧的原因是: 。 |
(1)改进后的图2装置与图1装置比较,优点是 。
(2)王泽同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是:
。
【拓展与迁移】
实验小结时,李颖同学说:“待a试管冷却恢复原温度后,如果将试管倒置水中,并在水中取下橡皮塞,将看到试管中液面升高。”这一说法得到大家的一致认同。
韩晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测:甲:接近试管容积的1/5;乙:小于试管容积的1/5。
你赞同的预测是 (填“甲”或“乙”),理由是:
。
【改进与实验】①4P + 5O2 2P2O5; ②没有氧气;③温度没有达到红磷的着火点。
2P2O5; ②没有氧气;③温度没有达到红磷的着火点。
【反思与评价】
(1) 阻止了磷燃烧生成的大量五氧化二磷向空气中扩散,避免了危害人体健康;(表述合理即可)
(2) 燃烧温度升高,气球膨胀,避免了试管塞的喷出。(表述合理即可)
【拓展与迁移】
甲;试管中的物质除了白磷,还有空气,白磷充足,燃烧结束,消耗完了空气中的氧气,所以是甲。
或乙:试管中的物质除了白磷,还有空气,白磷不充足,燃烧结束,没有消耗完空气中的氧气,所以是乙。
(表述合理即可)
解析试题分析:【改进与实验】根据燃烧的条件分析,燃烧必须同时满足三个条件:①要有可燃物,②可燃物要与氧气充分接触,③温度达到可燃物的着火点及以上;所以投入水中的白磷虽然温度达到着火点,但是在水中与空气隔绝,没有氧气不会燃烧;试管中的白磷能燃烧生成五氧化二磷,即4P+5O2 2P2O5,是因为它的温度达到了其着火点,又与空气接触,满足燃烧的条件;试管中的红磷尽管与空气接触,但是温度没有达到它的着火点,所以不会燃烧。
2P2O5,是因为它的温度达到了其着火点,又与空气接触,满足燃烧的条件;试管中的红磷尽管与空气接触,但是温度没有达到它的着火点,所以不会燃烧。
【反思与评价】(1)改进后的图2装置与图1装置比较,燃烧反应可以在较密闭的空间内完成,所以燃烧后的产物会留在试管中,不会散发到空气里,也就是说能防止白磷燃烧产生的五氧化二磷逸散,危害人体健康;
(2)由于燃烧反应会放出大量的热,而使试管内的气体膨胀,导致压强增大,图2装置中的橡皮塞会因此而松动,甚至冲出;图3装置中气球可随气体的膨胀而变大,避免了橡皮塞因试管内气体热膨胀而松动。
【拓展与迁移】由于空气中氧气约占空气体积的1/5,如果白磷足量、气密性良好,试管中的氧气能消耗完,则进入a试管内液体的体积能接近试管容积的1/5;若装置的气密性不严,即装置漏气的情况下,或白磷的量不足,不能完全反应掉空气中的氧气时,那么进入a试管内液体的体积要小于试管容积的1/5,所以要保证进入试管的水接近试管容积的1/5的前提条件是要保证装置的气密性良好,白磷足量等因素。
考点:燃烧的条件与灭火原理探究,化学实验方案设计与评价
点评:解答本题的关键是,理解和熟练掌握可燃物燃烧的条件,而且要明确,只有同时满足三个条件,物质才可以燃烧;另外对于装置优越性的改进,一般要考虑到操作的简便性,气密性良好,反应易操控,环境保护等方面。

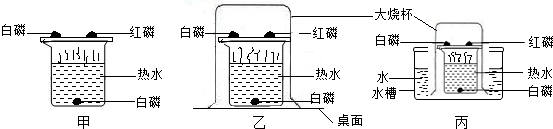
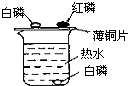 为了探究燃烧的条件,我们设计如下实验:实验装置如图所示,在250mL烧杯中,注入200mL热水,并投入一小块白磷,烧杯口盖上薄铜片,铜片一端放一小块已用滤纸吸干水的白磷,另一端放一小堆红磷(白磷着火点为40℃,红磷着火点为200℃).不一会儿,观察到:
为了探究燃烧的条件,我们设计如下实验:实验装置如图所示,在250mL烧杯中,注入200mL热水,并投入一小块白磷,烧杯口盖上薄铜片,铜片一端放一小块已用滤纸吸干水的白磷,另一端放一小堆红磷(白磷着火点为40℃,红磷着火点为200℃).不一会儿,观察到:
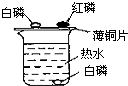 为了探究燃烧的条件,我们设计如下实验:实验装置如图所示,在250mL烧杯中,注入200mL热水,并投入一小块白磷,烧杯口盖上薄铜片,铜片一端放一小块已用滤纸吸干水的白磷,另一端放一小堆红磷(白磷着火点为40℃,红磷着火点为200℃).不一会儿,观察到:
为了探究燃烧的条件,我们设计如下实验:实验装置如图所示,在250mL烧杯中,注入200mL热水,并投入一小块白磷,烧杯口盖上薄铜片,铜片一端放一小块已用滤纸吸干水的白磷,另一端放一小堆红磷(白磷着火点为40℃,红磷着火点为200℃).不一会儿,观察到: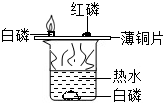 为了探究燃烧的条件,我们设计如下实验:实验装置如图所示,在250mL烧杯中,注入200mL热水,并投入一小块白磷,烧杯口盖上薄铜片,铜片一端放一小块已用滤纸吸干水的白磷,另一端放一小堆红磷(白磷着火点为40℃,红磷着火点为200℃).
为了探究燃烧的条件,我们设计如下实验:实验装置如图所示,在250mL烧杯中,注入200mL热水,并投入一小块白磷,烧杯口盖上薄铜片,铜片一端放一小块已用滤纸吸干水的白磷,另一端放一小堆红磷(白磷着火点为40℃,红磷着火点为200℃).