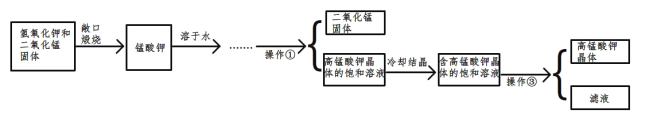
题目内容
【题目】下图分别是甲、乙两个实验小组,分别进行“加热硫酸铜和氢氧化钠两种溶液反应后的混合物”的实验过程及实验现象的示意图:
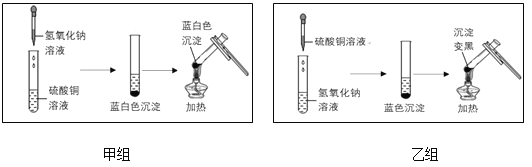
【甲组】氢氧化钠与硫酸铜反应的化学方程式为_______,加热两种溶液反应后的混合物,生成的黑色物质是氧化铜。
【乙组】为寻找两种溶液反应后的混合物在加热后没有产生氧化铜的原因,他们进行了以下实验探究:
【查阅资料】
a.氢氧化铜受热分解生成氧化铜和水。
b.在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:
6NaOH+4CuSO4=3Na2SO4+Cu4(OH)6SO4↓,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解。
【提出猜想】根据资料分析,乙组同学认为本组实验中氢氧化钠溶液不足,导致试管中溶液偏酸性的原因可能是:
猜想Ⅰ:过量的硫酸铜导致溶液呈酸性 猜想Ⅱ:生成的硫酸钠使溶液呈酸性。
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH______7(填“>”、“<”或“=”),硫酸铜溶液呈酸性,猜想Ⅰ成立。
实验②:向盛有硫酸钠溶液的试管中滴加石蕊溶液,观察到溶液仍显紫色,硫酸钠溶液呈________(填“酸性”、“中性”或“碱性”),猜想Ⅱ不成立。
【交流与反思】(1)乙组同学认真分析甲组实验后,认为不需要通过实验也能判定猜想Ⅱ不成立,理由是__________________________________________________。
(2)甲、乙两组实验说明相同的反应物会因其质量比的不同而可能导致_____不同。
【答案】 CuSO4+2NaOH=Cu(OH)2↓+ Na2SO4 PH<7 中性 甲组实验中也生成了Na2SO4,若它显酸性,在此条件下CuSO4和NaOH也会生成蓝白色沉淀 (或若 Na2SO4显酸性,甲组实验中不可能生成蓝色沉淀Cu(OH)2,因为Cu(OH)2与酸性溶液会反应) 生成物不同(或实验现象不同)
【解析】【甲组】根据反应物、生成物及化学方程式的书写规则分析解答;
【实验与结论】实验①根据溶液的pH与酸碱性的关系分析解答;
实验②根据石蕊溶液遇酸碱性不同的溶液显示的颜色分析解答;
【交流与反思】(根据实验现象分析解答。
解:【甲组】氢氧化钠与硫酸铜反应的化学方程式为 2NaOH+CuSO4= Na2SO4+ Cu(OH)2↓;
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH ﹤7(填“﹥”、“﹤”或“﹦”),硫酸铜溶液呈酸性,猜想Ⅰ成立。
实验②:向盛有硫酸钠溶液的试管中逐滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈中性(填“酸”、“中”或“碱”),猜想Ⅱ不成立。
【交流和反思】(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立,理由是甲组实验中也生成了Na2SO4,若它显酸性,在此条件下CuSO4和NaOH也会生成蓝白色沉淀(或若 Na2SO4显酸性,甲组实验中不可能生成蓝色沉淀Cu(OH)2,因为Cu(OH)2与酸性溶液会反应);
(2)在化学反应中,相同的反应物因质量比不同可能会导致生成物不同(或实验现象不同)。

【题目】实验室中有一瓶含有少量氯化钠和可溶性杂质的硫酸钠样品.某化学兴趣小组对该样品成分进行定量测定,甲、乙、丙三位同学分别称取一定质量的样品放入烧杯中,溶入足量水后过滤得到滤液;再向滤液中加入一定质量的氯化钡溶液,充分反应后过滤,将沉淀洗涤、干燥并称量.相关实验数据记录如下:(Na2SO4+BaCl2=BaSO4↓+2NaCl)
称量项目 | 甲 | 乙 | 丙 |
所取样品的质量/g | 15 | 15 | 20 |
加入氯化钡溶液的质量/g | 150 | 100 | 100 |
反应后所得沉淀的质量/g | 23.3 | 23.3 | 23.3 |
请回答下列问题:
(1)__________同学(选填“甲”“乙”或“丙”)所取用的样品与氯化钡溶液恰好完全反应.
(2)计算该样品中硫酸钠的质量分数.(写出计算步骤,计算结果保留到0.1%)
(3)若欲计算出样品与氯化钡溶液恰好完全反应时所得溶液的溶质质量分数,上述实验过程中还需要测定的数据是__________.
【题目】化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐酸中,有气泡产生,写出产生气泡的化学方程式______。
充分反应后静置,发现试管中有灰白色沉淀。
【提出问题】
灰白色沉淀是什么物质?
【猜想假设】
小华认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小华的猜想,理由是_。
小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体。
小彤认为灰白色沉淀为脱落的镁粉细颗粒。
【实验探究1】
实验操作 | 现象 | 结论 |
①取试管中的上层清液,加入适量的氯化镁固体 | 氯化镁固体 (选填“溶解”或“不溶解”) | 小宇猜想错误 |
②取适量白色沉淀加入足量稀盐酸中 | ______(选填“有”或“没有”)气泡冒出 | 小彤猜想错误 |
基于以上探究与分析,原有猜想均遭到了否定。
【查阅资料】
HCl+AgNO3═HNO3+AgCl↓,AgCl是一种白色沉淀。
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了______气体。再将湿润的石蕊试液浸泡过的滤纸条悬于试管口,试纸变______色。
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀。据文献介绍,碱式氯化镁的化学通式可表示为Mgx(OH)yClz,其不溶于水,能与酸反应。
【反思拓展】
(1)做镁与稀盐酸反应的实验时,镁条的用量宜少不宜多。
(2)铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活动性比铜______。还可根据铁和硫酸铜溶液的反应来确定这两种金属的活动性强弱,该反应的化学方程式为______。
(3)取一定量的碱式氯化镁沉淀【Mgx(OH)yClz】,溶于稀硝酸,将所得溶液分成两等份。
①向一份溶液中滴加过量的NaOH溶液,生成了1.16gMg ( OH )2沉淀;
②向另一份溶液中滴加过量的AgNO3溶液,生成了1.435 g沉淀。
通过计算得知:x:z=_________,所得碱式氯化镁的化学式为_________。
【题目】在校园科技节上,为测出鸡蛋壳(主要成分是碳酸钙)中钙元素的质量分数,
某同学称取已洗净、晾干、研成粉末的鸡蛋壳10克置于烧杯中,将烧杯放在电子天平上,往烧杯中加入100g的稀盐酸,每0.5分钟记录一次电子天平的示数,据此计算出产生气体的质量,具体数据如表:
时间(分钟) | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余物质质量(克) | 110 | 108.2 | 107 | 106.4 | 106.04 | 106.04 | 106.04 |
(1)若产生的气体全部是鸡蛋壳中的碳酸钙与盐酸反应生成的CO2,根据实验结果计算出该鸡蛋壳中钙元素的质量分数。(假定鸡蛋壳中其它成分不含钙元素,写出具体计算过程)________
(2)下列哪些情况会导致实验中钙元素质量分数测量结果偏大?_______
A.鸡蛋壳未晾干 B.鸡蛋壳未充分研碎
C.鸡蛋壳中含有碳酸镁(可与盐酸反应生成MgCl2、H2O和CO2)