题目内容
【题目】如图所示,某兴趣小组的同学为了探究酸碱盐之间能否发生反应做了以下几组实验。回答下列问题:
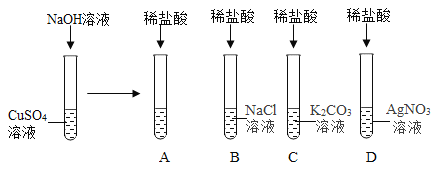
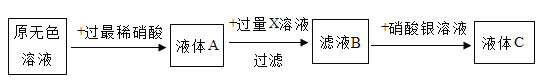
(1)向硫酸铜溶液中滴入氢氧化钠溶液,观察到的现象为_____,该反应的化学方程式为_____,继续滴加稀盐酸,通过稀盐酸与_____反应的现象证明了酸能与碱发生反应。
(2)B试管中无明显现象,不能发生复分解反应,理由是_____。
(3)观察到C试管中有_____生成,于是得出结论:稀盐酸能与碳酸钾发生反应。
(4)在D试管中有白色沉淀生成,于是得出结论:稀盐酸能与硝酸银发生反应。反应的化学方程式为_____。
(5)同学们对反应后C试管中溶液的溶质成分进行分析,得出以下结论
结论一:KCl
结论二:KCl、HCl;
结论三:_____。
某同学通过以下两种方法验证结论二是正确的。
实验操作 | 实验现象 | 实验结论 |
方法一:取C中溶液少许,加入足量的AgNO3溶液 | 产生白色沉淀 | 结论二正确 |
方法二:取C中溶液少许,加入适量的_____。 | 溶液颜色变红 |
(6)有些同学对方法一提出质疑,认为方法一不正确,理由是_____。当我们对反应后所得溶液的溶质成分进行猜想时,除了考虑生成物外,还要考虑_____。
【答案】产生蓝色沉淀 2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ 氢氧化铜 不符合复分解反应发生的条件 气泡 HCl+AgNO3=AgCl↓+HNO3 KCl、K2CO3 紫色石蕊试液 溶液中的氯化钾也能与硝酸银反应生成了氯化银白色的沉淀 过量
【解析】
(1)向硫酸铜溶液中滴入氢氧化钠溶液,硫酸铜与氢氧化钠反应生成了氢氧化铜沉淀和硫酸钠,所以观察到的现象为产生蓝色沉淀,该反应的化学方程式为:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓,继续滴加稀盐酸,通过稀盐酸与氢氧化铜反应的现象证明了酸能与碱发生反应。故填:产生蓝色沉淀;2NaOH+CuSO4═Na2SO4+Cu(OH)2↓;氢氧化铜
(2)B试管中无明显现象,不能发生复分解反应,理由是相互交换成分无气体、沉淀或水生成,不符合复分解反应发生的条件。故填:不符合复分解反应发生的条件
(3)由于碳酸钾能与稀盐酸反应生成了二氧化碳气体,所以观察到C试管中有气泡生成,于是得出结论:稀盐酸能与碳酸钾发生反应。故填:气泡
(4)在D试管中有白色沉淀生成,于是得出结论:稀盐酸能与硝酸银发生反应。反应的化学方程式为:HCl+AgNO3=AgCl↓+HNO3。故填:HCl+AgNO3=AgCl↓+HNO3
(5)由题意可知,C试管中发生的反应是碳酸钾与稀盐酸反应生成了氯化钾、二氧化碳和水,在分析反应后溶液中的溶质的成分时,除了考虑生成物外,还要考虑反应物是否过量,所以结论三为:KCl、K2CO3;由结论正确,即溶质为盐酸和碳酸钾,由实验现象为溶液变红,可推出向C溶液中加入的是紫色石蕊试液;故填:KCl、K2CO3
(6)有些同学对方法一提出质疑,认为方法一不正确,理由是溶液中的氯化钾也能与硝酸银反应生成了氯化银白色的沉淀。当我们对反应后所得溶液的溶质成分进行猜想时,除了考虑生成物外,还要考虑反应物是否过量。故填:溶液中的氯化钾也能与硝酸银反应生成了氯化银白色的沉淀;过量

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案【题目】现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.
(查阅资料)(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg﹣24、Fe﹣56、Zn﹣65
(实验步骤及数据)取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸的质量/g | 35.O | 35.0 | 35.O | 35.O |
剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
通过计算(写出计算过程),求:
(1)该混合物粉末中铜的质量分数?
(2)该混合物粉末中另一金属为何种金属?
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?