题目内容
【题目】硫酸是化工生产中重要的酸,其产量最大,用途最广,消耗量最多。历史上曾将硫酸的产量或消耗量作为一个国家化工生产发达程度的标志。
浓硫酸具有吸水性、脱水性和强氧化性。浓硫酸的腐蚀性主要是由它的脱水性和强氧化性引起的。稀硫酸有强酸性,稀硫酸的腐蚀性则主要是由酸性及水分蒸发后变浓而产生的。
硫酸的用途极广,常用于生产化肥、冶炼金属、农药、制药等。
工业制硫酸的流程为:FeS2![]() SO2
SO2 SO2
SO2 H2SO4
H2SO4
(1)综合分析以上材料,并结合已有知识,请回答:
①工业制H2SO4可能会引起的环境问题是_____。
②在实验室中不慎将浓硫酸沾到皮肤上的处理方法是_____。
A 立即用大量水冲洗,然后再涂上3%~5%的碳酸氢钠溶液。
B 立即用稀氢氧化钠溶液冲洗,然后再用水冲洗。
(2)某工厂化验室用9.8%的稀硫酸洗涤一定量化工产品中残留Ba(OH)2,当消耗稀硫酸100g时,沉淀不再产生,此时液体的pH=7(不考虑其它物质的影响),求化工产品中残留Ba(OH)2的质量。_____
【答案】形成酸雨(或造成空气污染) A 17.1g
【解析】
(1)①工业制H2SO4过程中,会向空气中排放二氧化硫气体,二氧化硫与水发生反应生成酸,使雨水的酸性增强,形成酸雨(或造成空气污染)。②在实验室中不慎将浓硫酸沾到皮肤上,要立即用大量水冲洗,然后再涂上显弱碱性的3%~5%的碳酸氢钠溶液 ,故选A。
(2)解:设化工产品中残留Ba(OH)2的质量为x。

![]()
解得x=17.1g
故填:17.1g

 应用题作业本系列答案
应用题作业本系列答案【题目】(10分)某校化学兴趣小组就空气中氧气的含量进行了分组实验探究。
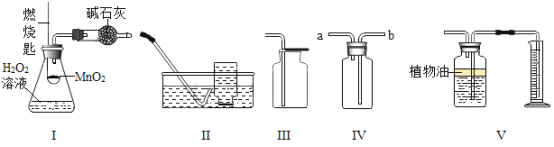
Ⅰ组:(1)Ⅰ组同学讨论后认为,选择的药品既要能消耗氧气,又不会跟空气中的其他成分反应而且生成物为固体。他们应该选择_________(填序号),为了充分消耗容器中的氧气,药品的用量应保证_______________________。
A.蜡烛 B.红磷 C.铁丝 D.木炭
(2)小组同学共同设计下图所示的两套装置,你认为合理的是______(填序号)。为了确保实验的成功,在装药品之前应该
____________________________________________。

(3)在讨论的基础上,他们分组进行了实验。
【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100 mL)
组别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积/mL | 20 | 21 | 19 | 20 | 22 | 19 |
(4)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的_________。
Ⅱ组:Ⅱ组同学发现Ⅰ组实验可能产生实验误差,对实验进行了改进,下图是Ⅱ组同学测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。
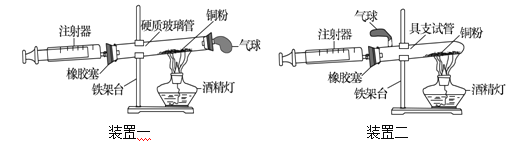
(1)根据下表提供的实验数据,完成下表
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
15mL | 15mL | 9mL |
(2)装置中气球的作用是 。
(3) 装置一和装置二中气球的位置不同, (填“装置一”或“装置二”)更合理,理由是 。
(4) 如何检查该装置的气密性? 。
【题目】如图所示,某兴趣小组的同学为了探究酸碱盐之间能否发生反应做了以下几组实验。回答下列问题:
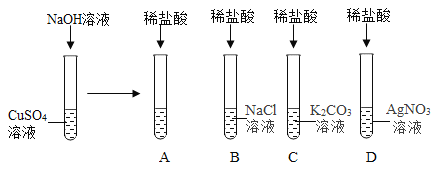
(1)向硫酸铜溶液中滴入氢氧化钠溶液,观察到的现象为_____,该反应的化学方程式为_____,继续滴加稀盐酸,通过稀盐酸与_____反应的现象证明了酸能与碱发生反应。
(2)B试管中无明显现象,不能发生复分解反应,理由是_____。
(3)观察到C试管中有_____生成,于是得出结论:稀盐酸能与碳酸钾发生反应。
(4)在D试管中有白色沉淀生成,于是得出结论:稀盐酸能与硝酸银发生反应。反应的化学方程式为_____。
(5)同学们对反应后C试管中溶液的溶质成分进行分析,得出以下结论
结论一:KCl
结论二:KCl、HCl;
结论三:_____。
某同学通过以下两种方法验证结论二是正确的。
实验操作 | 实验现象 | 实验结论 |
方法一:取C中溶液少许,加入足量的AgNO3溶液 | 产生白色沉淀 | 结论二正确 |
方法二:取C中溶液少许,加入适量的_____。 | 溶液颜色变红 |
(6)有些同学对方法一提出质疑,认为方法一不正确,理由是_____。当我们对反应后所得溶液的溶质成分进行猜想时,除了考虑生成物外,还要考虑_____。