题目内容
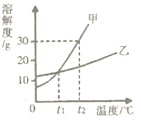
【题目】如图所示,在盛有冷水的烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增多,需向烧杯中加入的物质是
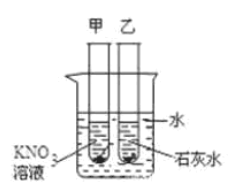
A.氯化钠B.氢氧化钠C.硝酸铵D.硝酸钾
【答案】B
【解析】
硝酸钾的溶解度随温度升高而升高,使其溶解应升温,而氢氧化钙的溶解度随温度升高而减小,使其析出需要也要升温。
A、氯化钠溶于水,溶于温度基本不变,甲、乙两支试管无变化,故A不正确;
B、硝酸钾的溶解度随温度升高而升高,氢氧化钙的溶解度随温度升高而减小,氢氧化钠溶于水放热,溶液温度升高,甲试管中晶体减少,乙试管中晶体增多,故B正确;
C、硝酸铵溶解时吸热,溶液温度降低,甲试管中晶体增多,乙试管中晶体减少,故C不正确;
D、硝酸钾溶于水,溶于温度基本不变,甲、乙两支试管无变化,故D不正确。故选B。

 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
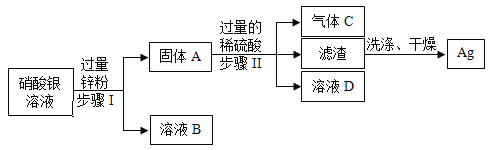
学练快车道口算心算速算天天练系列答案【题目】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图:
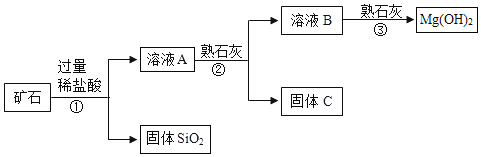
已知氢氧化铜、氢氧化铁和氢氧化镁均是沉淀,请回答下列问题:
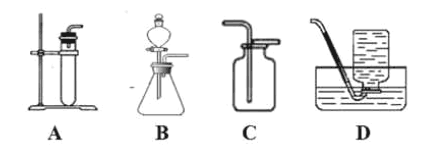
(1)步骤①和步骤②均用到的操作是__________,需要的玻璃仪器有烧杯、漏斗和_____________。
(2)溶液 A 中所含的阳离子有 Fe3+、Cu2+、Mg2+和 __________(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH 见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的 pH 范围为_______________;固体 C 中所含固体成分的化学式为______________;该步骤②中所涉及的中和反应的化学方程式是______________。
(4)步骤③制取 Mg(OH)2的化学方程式为______________。