题目内容
【题目】某工厂排出的废水中含有硝酸银,为了回收废水中的贵金属银,工厂进行了如下的操作。
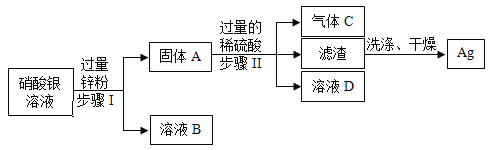
(1)锌的金属活动性比银的金属活动性______(选填“强”或者“弱”),固体A的成分有______,气体C的化学式是______。
(2)操I、Ⅱ的名称是______,该操作中需要用到的玻璃仪器有烧杯、漏斗和______。
(3)若往溶液E中加入适量的氧化锌,可得到只含有一种溶质的溶液,则发生反应的化学方程式为______。
【答案】强 银、锌 H2 过滤 玻璃棒 ZnO+H2SO4=ZnSO4+H2O
【解析】
解:(1)锌的金属活动性比银的金属活动性强,固体A的成分有反应生成的银河过量的锌,气体C是锌和稀硫酸反应生成的氢气,氢气的化学式是H2。
故填:强;银、锌;H2。
(2)操I、Ⅱ的名称是过滤,该操作中需要用到的玻璃仪器有烧杯、漏斗和玻璃棒。
故填:过滤;玻璃棒。
(3)若往溶液E中加入适量的氧化锌,氧化锌和稀硫酸反应生成硫酸锌和水,可得到只含有一种溶质硫酸锌的溶液,则发生反应的化学方程式为:ZnO+H2SO4═ZnSO4+H2O。
故填:ZnO+H2SO4═ZnSO4+H2O。
硝酸银和锌反应生成硝酸锌和银;
稀硫酸和锌反应生成硫酸锌和氢气,和氧化锌反应生成硫酸锌和水。
本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案【题目】小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】
(1)6H2SO4(浓)+2Fe![]() Fe2(SO4)3+6H2O+3SO2↑
Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产生可能有二氧化硫
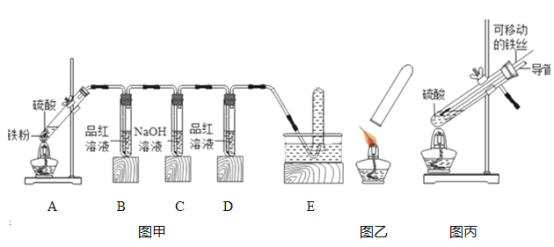
【实验探究】小明用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
(1)请帮助小明完成下表:
实验现象 | A中生成气体成分 | ||||
B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
实验一 | 98% | ________ | 不褪色 | 无爆鸣声 | 只有SO2 |
实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ________ |
实验三 | 25% | ________ | 不褪色 | ________ | 只有H2 |
【实验结论】铁与不同浓度的硫酸反应,生成的气体产物可能不同,当硫酸溶液浓度达到足够大时,生成的气体产物中有二氧化硫.
(2)【实验结论】铁与不同浓度的硫酸反应,生成的气体产物可能不同,当硫酸溶液浓度达到足够大时,生成的气体产物中有二氧化硫
【交流反思】
(1)写出实验三中铁与硫酸溶液反应的化学方程式 ________ ,写出实验二中发生爆鸣反应的化学方程式________ .
(2)实验一中C装置的作用是________ .
【拓展延伸】小明又将A装置进行了如图所示的改进,试分析:增加的导管下端伸入液面以下原因________ ,该导管所起的作用是_________ .
【题目】根据下列实验装置图,回答下列问题。
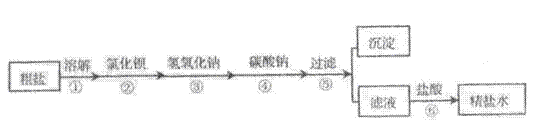
我国制碱工业的先驱侯德榜发明了将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献,其生产工艺流程示意图如图:
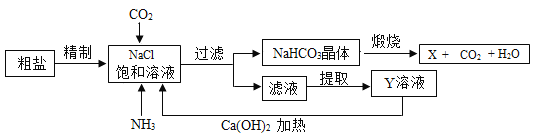
(查阅资料)粗盐中含有CaCl2、MgCl2等可溶性杂质。
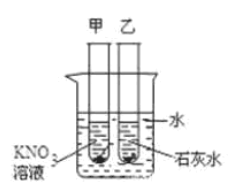
科学探究是学习化学的一种科学方法。 下面是某小组在学习复分解反应时呈现的一组探究实验。向盛有少量硫酸铜溶液的两支试管中分别加入氢氧化钠溶液和氯化钡溶液同学们在探究金属的化学性质时,老师强调一般不用K、Ca、Na等活泼金属,否则会出现异常现象,并对钾和硫酸铜溶液的反应进行了演示实验。
(资料显示)
a.钾在常温下就能与水发生剧烈的反应,请补充完整发生反应的化学方程式:2K+2H2O=2_____+H2↑。
b.碱式铜盐为蓝绿色沉淀。
c.钾在空气中其表面很快会被氧化。
(提出猜想)
猜想一:金属钾和硫酸铜溶液反应会有铜生成。
猜想二:金属钾和硫酸铜溶液反应,生成的沉淀只有氢氧化铜。
(实验及现象)切取不同大小的钾块分别投入两种不同浓度的硫酸铜溶液中,有关实验现象如表所示:
实验及现象
实验编号 | 钾块大小 | 硫酸铜溶液 | 实验现象 |
① | 绿豆大小 | 稀溶液10 mL | 产生蓝绿色沉淀 |
② | 绿豆大小 | 浓溶液10 mL | 产生蓝色絮状沉淀 |
③ | 黄豆大小 | 稀溶液10 mL | 产生蓝色絮状沉淀 |
④ | 黄豆大小 | 浓溶液10mL | 产体生蓝色絮状沉淀,并出现黑色固体 |
(实验结论)
氧化亚铜(Cu2O)可用于生产船底防污漆,防止海洋生物对船舶设备造成污损。现将Cu2O和Cu的混合物36g 放入烧杯中,加入质量分数为14.7%的稀硫酸100g,恰好完全反应(已知:Cu2O+H2SO4=CuSO4+Cu+H2O)。请计算:
(1)所加稀硫酸中溶质的质量为_____g。
(2)原混合物中Cu2O的质量。_____(写出计算过程)
【题目】根据下表回答问题.
已知某物质在不同温度下的溶解度数据如表所示:
温度(℃) | 0 | 20 | 40 | 60 | 80 |
溶解度(克) | 12.6 | 15.3 | 20.0 | 25.0 | 42 |
(1)40℃时,150克水最多能溶解该物质的质量是_____g;
(2)如果要配制该物质溶质质量分数为20%的饱和溶液200克,需要水_____ g,此时溶液的温度应为_____℃;
(3)在20℃时,将40g该物质加入到100g水中,能形成溶液_____g,再将此溶液升温到80℃,此时溶液成为_____(填“饱和”或者“不饱和”)溶液。