题目内容
【题目】金属材料与生产生活紧密联系
(1)下列选项为金属材料的有___________。
A 塑料 B腈纶 C铝粉 D氧化镁 E金刚石 F铝锂合金
(2)同学们用“W”型玻璃管进行实验室模拟炼铁的实验,如下图所示。
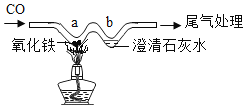
①a处固体颜色如何变化__________?
②b处澄清石灰水的作用是什么__________?
③若证明反应后a处固体中含有单质铁,请设计简单实验方案__________。
(3)探究小组的同学利用下图装置验证某混合气体中是否含有CO2和CO。
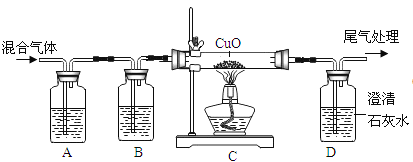
①A、B装置中应分别盛放什么试剂__________?
②若原混合气体中含有CO,可观察到什么实验现象__________?
③写出D中可能发生反应的化学方程式__________。
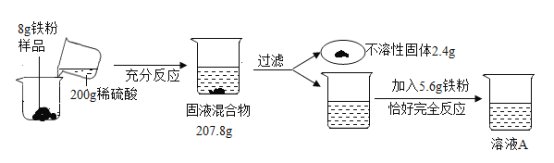
(4)取10g氯化钠溶液于烧杯中,加入足量的硝酸银溶液,充分应用后过滤,洗涤烘干后得到2.87g固体。请计算该氯化钠溶液中溶质的质量__________。
【答案】CF 红棕色变为黑色 检验二氧化碳 取少量固体与试管中,滴加少量稀盐酸,若溶液中有气泡产生且溶液由无色变为浅绿色,则证明是单质铁。 澄清石灰水,氢氧化钠溶液 装置C中黑色固体变为紫红色,装置D中长导管有气泡冒出且澄清石灰水变白色浑浊 ![]() 1.17g
1.17g
【解析】
(1)金属材料有纯金属及它们的合金,故填:CF。
(2)①a处是氧化铁与一氧化碳反应生成铁和二氧化碳,固体颜色如何变化红棕色变为黑色,故填:红棕色变为黑色。
②澄清石灰水的作用是检验二氧化碳,故填:检验二氧化碳。
③若证明反应后a处固体中含有单质铁,应该利用铁的化学性质,能与稀盐酸反应,取少量固体与试管中,滴加少量稀盐酸,若溶液中有气泡产生且溶液由无色变为浅绿色,则证明是单质铁,故填:取少量固体与试管中,滴加少量稀盐酸,若溶液中有气泡产生且溶液由无色变为浅绿色,则证明是单质铁。。
(3)①A装置中的试剂需要检验二氧化碳的存在,所以应该放入澄清的石灰水;B装置的试剂除去多余的二氧化碳,防止对一氧化碳产物的干扰,因此可以是氢氧化钠溶液;
②若原混合气体中含有CO,可观察到装置C中黑色固体变为紫红色,装置D中长导管有气泡冒出且澄清石灰水变白色浑浊,故填:装置C中黑色固体变为紫红色,装置D中长导管有气泡冒出且澄清石灰水变白色浑浊。
③D中是二氧化碳与澄清石灰水反应生成碳酸钙和水,其化学方程式是![]() ,故填:
,故填:![]() 。
。
(4)设氯化钠的质量为x。

![]()
x=1.17g
故该氯化钠溶液中溶质的质量为1.17g。

【题目】用“盐酸—硫酸钡法”生产BaCl2会放出有毒气体H2S(其水溶液有酸性),可用NaOH吸收H2S制取Na2S进行处理。(相关反应的化学方程式:H2S+2NaOH=Na2S+2H2O)
项目 | 单价(元/吨) |
NaOH | 2500 |
Na2S | 5000 |
辅助费用(以处理1吨H2S计) | 1114 |
(1)若某化工厂每天要处理10吨H2S,需消耗NaOH多少吨_____?
(2)下表为H2S回收工艺的各项生产成本:
根据上述资料分析,从经济效益考虑这种处理H2S的方法是___(选填“盈利”或“亏损”)的。
【题目】请从 A 或B 两题中任选一个作答,若两题均作答,按 A 计分。
在一定条件下,Mg 和 MgH2的相互转化可以实现氢气的储存和释放。其工作原理如图。
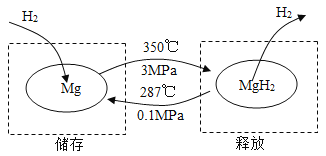
A | B |
(1)氢气储存时发生反应的化学方程式为_______。 (2)氢气很容易逃逸,若氢气存储效率为 10%,储存 1 kg 氢气,至少需要 Mg 的质量为_______ kg。 | (1)氢气释放时发生反应的化学方程式 为_______。 (2)理论上,52 kg MgH2最多能释放氢气的质量为_______ kg。 |