题目内容
【题目】是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
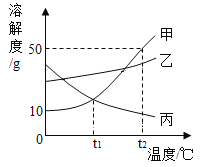
A. t1℃时,甲与丙两种物质的饱和溶液中溶质质量相同
B. 乙中混有少量甲时,应采用降温结晶的方法提纯乙
C. t2℃时,30g 甲能溶解于 50g 水中形成 80g 溶液
D. t2℃时,甲、乙、丙的饱和溶液降温到 t1℃时,其溶质质量分数大小为:乙>甲>丙
【答案】D
【解析】
A、t1℃时,甲与丙两种物质的饱和溶液的质量不能确定,所以饱和溶液中溶质质量不能确定,故A错误;
B、乙物质的溶解度受温度变化影响较小,所以乙中混有少量甲时,应采用蒸发结晶的方法提纯乙,故B错误;
C、t2℃时,甲物质的溶解度是50g,所以30g甲能溶解于50g水中形成75g溶液,故C错误;
D、t1℃时,乙物质的溶解度最大,甲、丙物质的溶解度相等,降低温度,甲、乙物质的溶解度减小,丙物质的溶解度增大,应该按照t2℃时的溶解度计算,所以t2℃时,甲、乙、丙的饱和溶液降温到 t1℃时,其溶质质量分数大小为:乙>甲>丙,故D正确。
故选D。

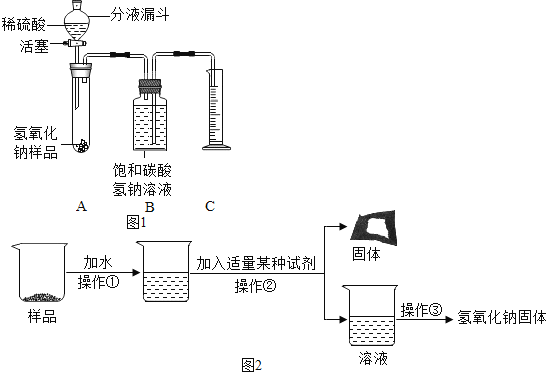
【题目】某山区盛产石灰石,其中含有的杂质为二氧化硅(不溶于水、高温下难以分解的酸性氧化物).S中学初三化学研究性学习小组的同学为了测定某矿山石灰石的纯度,取2.0g该矿山石灰石样品,将20.0g盐酸平均分成4份,分4次入到样品中,充分反应后测定剩余固体的质量,数据见表.试求:
次数 | 1 | 2 | 3 | 4 |
加入盐酸质量/g | 5.0 | 5.0 | 5.0 | 5.0 |
剩余固体质量/g | 1.3 | 0.6 | 0.2 | 0.2 |
(1)2.0g石灰石样品中杂质的质量.
(2)石灰石样品中碳酸钙的质量分数.
(3)加入的盐酸中溶质的质量分数是多少?
【题目】溶液与人们的生产生活密切相关。
(1)如表是KNO3在不同温度时的溶解度,回答问题。
温度/℃ | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 |
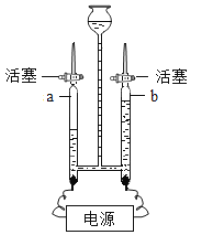
90℃时,将一定质量的KNO3溶液按图1示进行操作:

90℃时的KNO3溶液是______(填“饱和”或“不饱和”)溶液。图中n的数值为______。
(2)请根据如图2中甲、乙、丙三种固体的溶解度曲线回答问题。
T3℃时,在各加有甲、乙、丙30克固体的三个烧杯中,分别倒入50克水,充分搅拌后,形成饱和溶液的是______当温度降低至T2℃时,此三杯溶液中溶质的质量分数由大到小的顺序为______。
T3℃时100克水中加入95克甲的固体,发现全部溶解,一段时间后又有部分甲的固体析出。“全部溶解”的原因可能是:______。