题目内容
【题目】在中考化学实验考查中,小华同学抽到的题目是“用盐酸中和氢氧化钠溶液”。
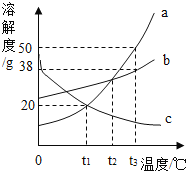
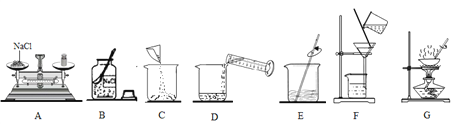
(1)小华完成该实验的部分操作过程如下图所示:

①小华上述操作过程中有明显错误的是____________(填字母序号)。
②操作B中,看到酚酞显________色,操作C中当看到________________________现象时说明氢氧化钠与盐酸发生了中和反应,反应方程式为________________________________
(2)实验考查结束后,化学兴趣小组的同学帮老师一起整理实验室。在整理废液缸时,发现废液缸中的溶液为无色,小娟同学提出,废液为中性。小敏不同意,她认为废液也可能是酸性,理由是________________。
(3)在整理实验台时,他们又看到了一个不和谐的“音符”(如图)。

①此情此景你首先想到的是它可能变质了,该变质反应的_____________________
②围绕此瓶NaOH溶液是否变质的问题,兴趣小组同学利用当时实验桌上的三种试剂(氯化钙溶液、稀盐酸、酚酞试液)展开了探究活动。
小娟取少量溶液于试管中,滴加某种试剂,有气泡产生,证明NaOH溶液已经变质。你认为小娟所加的试剂是_______________
小明欲证明变质的溶液中尚存NaOH,请你帮助小明完成以下探究方案:
探究目的 | 探究步骤 | 预计现象 |
除尽溶液中的CO32- | ①:取少量溶液于试管中,滴加足量的__________试剂 | 有白色沉淀产生 |
证明溶液中尚存NaOH | ②:向实验①所得溶液中滴加酚酞试液 | ____________ |
通过上述探究,说明氢氧化钠溶液暴露在空气中容易变质,故应密封保存。
【答案】 A 红色 红色褪去 NaOH+HCl===NaCl+H2O 溶液为酸性,酚酞也是无色 2NaOH+CO2=Na2CO3+H2O; 稀盐酸 CaCl2溶液 酚酞变红色
【解析】(1)①使用细口瓶倾倒液体药品,操作要领是“一放、二向、三挨、四流”,即先拿下试剂瓶塞倒放在桌面上,然后拿起瓶子,瓶上标签向着手心,瓶口紧挨着试管口,让液体沿试管内壁慢慢地流入试管底部,而小华把试剂瓶塞随便放置,这样会污染瓶内试剂;其他实验操作没有错误;②向氢氧化钠溶液滴加酚酞,溶液会变红,再滴加稀盐酸,盐酸会与氢氧化钠反应,完全反应后红色消失,反应方程式为:NaOH+HCl=NaCl+H2O;(2)在酸性环境下,酚酞溶液仍为无色;(3)①NaOH溶液易吸收空气中的二氧化碳生成Na2CO3,故该变质反应的方程式为:2NaOH+CO2═Na2CO3+H2O;②盐酸可与碳酸钠反应生成二氧化碳气体;探究方案:①Na2CO3+CaCl2=CaCO3↓+2NaCl,那么在少量NaOH溶液中加入足量CaCl2溶液后,产生白色沉淀,就除尽了CO32-;②氢氧化钠可使酚酞试液变红。