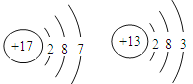��Ŀ����
����Ŀ����13�֣���������װ��ͼ�ش����⣺

��1�����Ϊ�ٵ����������� ��
��2��ע����H�����ڼ��װ��B�������ԣ��������£�
������ƿ�м�������ˮ�� ����
�ڽ�ע����H���ӵ�װ��B�ĵ��ܿڴ���
�ۻ�����������ע����H�Ļ������۲쵽 ����ʾװ��B�����������á�
��3��ʵ��������ˮ�����ƺͼ�ʯ�ҵĻ�Ϲ����ڼ�����������ȡ�������壬�䷢��װ�ÿ�ѡ�� ������ĸ��ţ������������ѡ��Eװ�ý����ռ����ռ�������ƿ�ķ��÷�ʽ����ͼ���ɴ˿��ƶϼ���һ���߱������������� �� ��
![]()
��4��ʵ������һ�������ĸ��������ȡ������ͨ����ˮ���ⶨ���ռ��������������װ��ѡ��A��F��G����
��д���÷�Ӧ�Ļ�ѧ����ʽ ��
������װ�õ�����˳���ǣ�a��b��c��d��Fװ���ڵ��ܣ���b����c�������������죿�뻭����
�۸��ݸ�����ص�����������������Ϊ����ֵ�����ʵ�ʲ�ã�ˮ���������ȷ��������Ϊԭ���� ��
��5������������غͶ�����������ȡ����������������ڷ�Ӧǰ����������е����������� ����������С�����䡱����ʵ��������װ��B��ȡO2ʱ������ע����H���泤��©�����ŵ��� ��
���𰸡���1������©����1�֣�
��2����û����©�����¶˿ڣ�1�֣� ����©�����¶˿�������ð����1�֣�
��3��A��1�֣� �����ѣ�������ˮ��1�֣��� �ܶȱȿ���С��1�֣�
��4���� 2KMnO4 ![]() K2MnO4��MnO2��O2�� ��2�֣�
K2MnO4��MnO2��O2�� ��2�֣�
����ͼ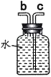 ��2�֣�
��2�֣�
��δ��ȴ�����¾Ͷ��� ��1�֣�
�ܱ����1�֣� ���Ʒ�Ӧ��������1�֣�
��������
�����������1���ԣ�
��2��Ҫ��������Լ�����ֻ�ܴӵ�����������ô�ͱ������©�����ij��ڣ������û����©�����¶˿�����ѹ��С��������©��������������ݣ�
��3����Ӧ�ﶼΪ�������������˷���װ��ΪA��ѡ��E��ˮ���ռ�˵��������ˮ��ƿ�ڳ���˵���ܶȱȿ���С��
��4�����ԣ���������b�ڽ���ˮ��c�ڳ��������ܶȱ�ˮС�����b��c������������ȡ�������������¶�ƫ����ʹ�������ͣ�ʵ�ʲ������������ͻ���������ֵ���������ȴ�������ڲ�������������ڶ������̴��¼��ȷֽ���������Ȼ��أ�������������С��������������Ϊ�����������䣬��ô�����������ͻ�����ע����H���Կ���Һ�����������ٶȽ������Ʒ�Ӧ�����ʣ�

 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�