题目内容
【题目】铝、铁、铜是我们生活中常见的金属.

甲同学 乙同学 丙同学
(1)铝制品具有很好的耐腐蚀性能,原因是 ________________________________ .
(2)铁生锈的条件是 ______________ ,生活中防止铁生锈的方法有 ___________(写一种即可).
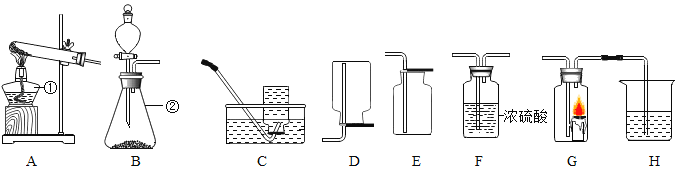
(3)为探究铝、铁、铜三种金属的活动性顺序,甲、乙、丙三位同学设计了如下实验方案(金属片已打磨),如上图所示:
①甲同学根据铜片表面无变化的现象,判断出三种金属的活动性顺序为Al>Fe>Cu.
②乙同学只用一支试管,取一次稀盐酸也能证明![]() 他在稀盐酸中插入金属的顺序为: ______ 或 ______ ,写出其中一个反应的化学方程式 ________________________ .
他在稀盐酸中插入金属的顺序为: ______ 或 ______ ,写出其中一个反应的化学方程式 ________________________ .
③丙同学把一定量的铁粉放入CuCl2和AlCl3的混合溶液中,充分反应后过滤,向滤出的固体中加入稀盐酸,无明显现象,则滤液中一定含有的溶质是 ______ .
【答案】铝与氧气在空气中反应生成致密的氧化铝薄膜 氧气、水 刷漆、涂油 Cu Fe Al Fe Cu Al Fe+2HCl=FeCl2+H2↑ AlCl3 、FeCl2
【解析】
铝和氧气生成氧化铝薄膜,饱和金属,金属生锈的条件:有水和氧气,铁和盐酸反应生成氯化亚铁和氢气,铝和盐酸反应生成氯化铝和氢气,铜和盐酸不反应,铝和氯化亚铁反应生成氯化铝和铁。
(1)铝制品具有很好的耐腐蚀性能,原因是铝与氧气在空气中反应生成致密的氧化铝薄膜。
(2)铁生锈的条件是氧气、水,生活中防止铁生锈的方法有刷漆、涂油。
(3) ①甲同学根据铜片表面无变化的现象,判断出三种金属的活动性顺序为Al>Fe>Cu。
②乙同学只用一支试管,取一次稀盐酸也能证明![]() 他在稀盐酸中插入金属的顺序为:Cu Fe Al 或 Fe Cu Al ,其中一个反应的化学方程式Fe+2HCl=FeCl2+H2↑
他在稀盐酸中插入金属的顺序为:Cu Fe Al 或 Fe Cu Al ,其中一个反应的化学方程式Fe+2HCl=FeCl2+H2↑
③丙同学把一定量的铁粉放入CuCl2和AlCl3的混合溶液中,充分反应后过滤,向滤出的固体中加入稀盐酸,无明显现象,则滤液中一定含有的溶质是AlCl3 、FeCl2。