题目内容
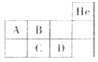
【题目】现有一包固体粉末,可能由![]() 、
、![]() 、
、![]() 中的一种或几种组成,为确定其成分,按下列流程进行实验。
中的一种或几种组成,为确定其成分,按下列流程进行实验。
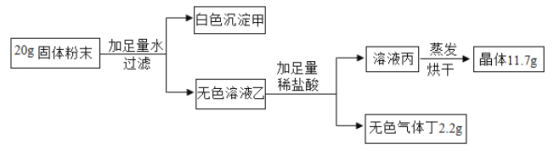
下列说法中正确的是( )
A. 白色沉淀甲是![]() 且一定是原固体粉末中的
且一定是原固体粉末中的![]()
B. 无色溶液乙中一定含有![]()
C. 固体粉末成分有二种可能的组成
D. 固体粉末是由![]() 、
、![]() 、
、![]() 组成的
组成的
【答案】BD
【解析】
碳酸钙难溶于水,氧化钙与水反应生成氢氧化钙,碳酸钠能溶于水,且能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠与盐酸反应生成氯化钠和水,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,由此可知最后得到的晶体是氯化钠。
A、根据分析可知,白色沉淀是碳酸钙,可能是原固体粉末中的碳酸钙,也有可能是氢氧化钙与碳酸钠生成的碳酸钙,故A错误;
B、无色溶液乙中加稀盐酸产生气体,故溶液乙中一定含有![]() ,故B正确;
,故B正确;
C、固体粉末中一定有碳酸钠,可能有氧化钙和碳酸钙中的一种或两种,根据分析知,生成的无色气体是二氧化碳,设与盐酸反应的碳酸钠的质量为x,生成的氯化钠的质量为y,

![]() ,x=5.3g
,x=5.3g
![]() ,y=5.85g,
,y=5.85g,
根据计算可知,晶体中有11.7g-5.85g=5.85g来自氢氧化钠与盐酸反应,根据质量守恒定律列关系式,设固体粉末中氧化钙的质量为m,与氢氧化钙反应的碳酸钠的质量为n,

![]() ,m=2.8g,n=5.3g,
,m=2.8g,n=5.3g,
粉末中碳酸钠的质量为:5.3g+5.3g=10.6g,氧化钙的质量为:2.8g,10.6g+2.8g=13.4g<20g,故粉末中还含有碳酸钙。固体粉末中只有这一种组成,故C错误;
D、根据以上选项中的分析可知,固体粉末是由![]() 、
、![]() 、
、![]() 组成的,故D正确。故选BD。
组成的,故D正确。故选BD。

 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案【题目】固体铵盐A、B的成分可能是(NH4)2SO4、NH4HSO4,或是两者的混合物.甲、乙两个研究性学习小组要确定A和B的成分,并测定B中氮元素的质量分数.
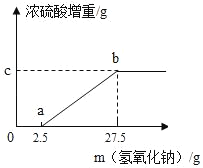
(1)甲实验小组的同学取了数份相同质量的样品A溶于水,然后加入40% NaOH溶液(图中用氢氧化钠质量表示),水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用足量浓硫酸完全吸收,浓硫酸增重的质量如图.分析该图象并回答下列问题:
①写出ab段涉及的化学方程式:_____.
②样品A的成分是_____,C点的数值是_____.
(2)乙实验小组的同学取了数份不同质量的样品B,测定方法与甲组同学大部分相同,不同的是,他们将不同质量的铵盐分别加入到50.00mL NaOH溶液中(含8.12g NaOH),测定结果如下:
实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
铵盐的质量(g) | 10.00 | 20.00 | 30.00 | 50.00 |
浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
①分析实验数据可知,实验编号为_____的实验中,氢氧化钠足量,铵盐中的铵根离子完全转化成气体.
②计算B中氮元素的质量分数.______(保留两位小数)