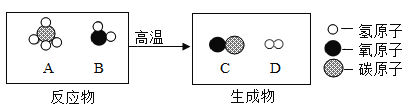
题目内容
【题目】设计实验、动手操作、观察现象、记录信息、提炼证据、进行推理、形成结论是化学学习的重要方法。
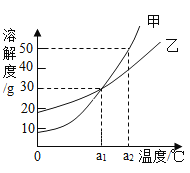
(1)学习化学概念“饱和溶液”——实验“KNO3溶于水”
[实验用品]KNO3(研磨处理)、水、玻璃棒、三脚架、石棉网、酒精灯、烧杯等。
[实验探究]在室温20℃下,向小烧杯中加入20mL水,按下表中设计的操作步骤进行实验。
实验序号 | 实验步骤 | 实验现象 | 实验推理 | 实验结论 |
I | 加入2gKNO3,搅拌 | 全部溶解 | 不一定形成饱和溶液 | 在一定温度下,一定量水中不能无限制地溶解溶质 |
Ⅱ | 再加入5gKNO3,搅拌 | 部分溶解 | _____ | |
Ⅲ | 加热,搅拌 | ____ | 不一定形成饱和溶液 | KNO3的溶解度随温度的升高而_________ |
Ⅳ | 再加入5gKNO3,搅拌 | 全部溶解 | 不一定形成饱和溶液 | |
Ⅴ | 放在冷水的大烧杯中冷却 | 析出晶体 | 一定形成饱和溶液 | KNO3可用__________的方法结晶 增加溶剂的质量,可将饱和溶液转化为不饱和溶液 |
Ⅵ | _______,搅拌 | 全部溶解 | 一定形成不饱和溶液 |
[实验反思]
①KNO3预先研磨处理的目的是____________________________。
②实验步骤_____________(填实验序号,下同)中KNO3的溶质质量分数最大。
③比较实验步骤 ___________中观察到的实验现象,经分析推理,可得出将KNO3饱和溶液转化为不饱和溶液的另一种方法,即升高饱和溶液的温度。
(2)应用化学知识“身边的化学”——体验“家庭燃料的变迁”[文献资料]
①天然气和煤都是___________(选填“可再生”或“不可再生”)能源;天然气的主要成分是_______(填化学式)。
②我国近50年来家庭燃料变迁:煤或木柴→液化石油气或管道煤气→天然气
③CO2能产生___________效应,SO2易导致酸雨。
④充分燃烧天然气和煤各1kg产生CO2和SO2的质量如下图所示。
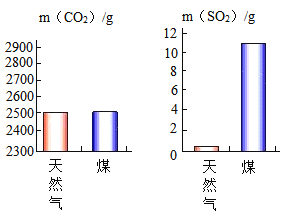
[证据推理]各级政府推广“利用天然气代替煤作家庭燃料”,分析文献资料可知实施该项举措的科学依据是_________________。
[联系实际]为防止燃气泄漏造成危险,使用天然气的家庭“将报警器安裝位置确定在燃气灶附近墙壁的上方”,这是基于天然气具有_______________的性质。
[反思拓展]保护生态环境是建设“人类命运共同体”的重要组成部分,我国科学家正在利用和开发H2等新能源,在一定程度上减少对环境的污染。请再列举一例可利用的新能源:______________。
【答案】一定形成饱和溶液 全部溶解 升高 降温 加入过量的水 增大接触而积,加速溶解 Ⅳ Ⅱ和Ⅲ 不可再生 CH4 温室 可以减少SO2的排放 密度比空气小 风能(太阳能等)
【解析】
(1)[实验探究]步骤Ⅱ.向小烧杯中加入2gKNO3全部溶解后,再加入5gKNO3,部分溶解,说明所得溶液一定是饱和溶液,故一定形成饱和溶液。
步骤Ⅲ.将小烧杯进行加热,推理得出不一定形成饱和溶液,则小烧杯中的固体已全部溶解,无法判断所得溶液是否饱和。
步骤Ⅳ. 向小烧杯中再加入5gKNO3,搅拌,固体全部溶解,无法判断所得溶液是否为饱和溶液。对比步骤Ⅱ、Ⅲ、Ⅳ可知,KNO3的溶解度随温度的升高而升高。
步骤Ⅴ. 将小烧杯放在盛有冷水的大烧杯中冷却,析出晶体,所得溶液一定是饱和溶液。结合实验Ⅳ和Ⅴ分析可知,KNO3可用降温的方法结晶。
步骤Ⅵ. 向小烧杯中加入过量的水,固体全部溶解,所得溶液为不饱和溶液,可推理得出结论:增加溶剂的质量,可将饱和溶液转化为不饱和溶液。
[实验反思]①为了增大固体和水的接触而积,加速溶解,实验前会将KNO3预先研磨处理。
②通过分析可知,实验步骤Ⅳ中KNO3的溶质质量分数最大。
③比较实验步骤Ⅱ和Ⅲ中观察到的实验现象,经分析推理,可得出将KNO3饱和溶液转化为不饱和溶液的另一种方法,即升高饱和溶液的温度。
(2)[文献资料]①天然气和煤都是化石燃料,属于不可再生能源;天然气的主要成分是甲烷,化学式为CH4。
③二氧化碳是导致温室效应的主要气体。
[证据推理]由图可知,充分燃烧天然气和煤各1kg,煤产生SO2的质量比天然气多,故各级政府推广“利用天然气代替煤作家庭燃料”的科学依据是可以减少SO2的排放。
[联系实际]因为甲烷的密度比空气小,所以为防止燃气泄漏造成危险,使用天然气的家庭“将报警器安裝位置确定在燃气灶附近墙壁的上方”。
[反思拓展]目前人类可利用的新能源有风能、太阳能、潮汐能等。

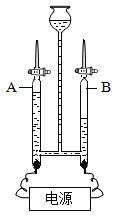
【题目】(1)如图是实验室制取气体的一些装置,据图回答:
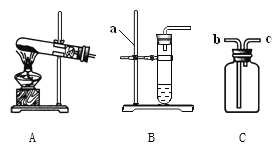
①图B中仪器a的名称是________________。
②用高锰酸钾制取氧气的发生装置是_____________(填序号),若用C装置手机氧气,验满时,应将带木星的木条放在_____________(填“b”或“c”)端导口,若木条复燃,说明氧气已满。
(2)小明在帮老师整理实验室时,发现一瓶为密封的KOH固体,对其成分提出以下假设,并在老师的指导下进行实验探究。
[查阅资料]:①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因是____________。
②K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性。
[猜想假设]:假设Ⅰ:只含KOH;假设Ⅱ:含KOH和K2CO3;假设Ⅲ:只含K2CO3
[进行实验]:
实验操作步骤 | 实验现象 | 实验结论 |
① 取少量样品于试管中,加入足量的稀盐酸 | 有气泡产生 | 假设______不正确 |
② 另取少量样品于试管中,加水溶解,加入过量的BaCl2溶液,振荡,静置 | ————————— | 假设Ⅲ正确 |
③ 取②中上层清液,滴加无色酚酞溶液 | ————————— |
[问题讨论]:步骤②中加入过量BaCl2溶液的作用是_____________________。
[拓展应用] :完全变质的KOH也有利用价值,从K2CO3的组成或性质看,这瓶变质的试剂在农业上的用途是_________________________________。