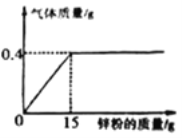
题目内容
【题目】向等体积含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如图1、图 2 所示,将图1与图2的阴影部分进行叠加,两者基本重合。下列说法正确的是( )

A. b 点的溶质为稀盐酸和氯化钠
B. c 点的溶质为氯化钠和碳酸钠
C. 由图可知碳酸钠在一定条件下可以转化成碳酸氢钠
D. 由图可知碳酸钠溶液的碱性比碳酸氢钠溶液的碱性弱
【答案】C
【解析】A、碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,b点时稀盐酸过量,因此溶质是反应生成的NaCl和过量的HCl,错误;B、将图1和图2的阴影部分进行叠加,发现两者基本重合,说明向碳酸钠溶液中加入稀盐酸时,碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,然后碳酸氢钠再和稀盐酸反应生成氯化钠、水和二氧化碳,因此c点的溶质是反应生成的NaCl和NaHCO3,错误;C、碳酸钠溶液中加入稀盐酸时,碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,正确;D、碳酸钠溶液中加入稀盐酸时,碳酸钠先和稀盐酸反应生成碳酸氢钠和氯化钠,pH值减小,所以碳酸钠溶液的碱性比碳酸氢钠溶液的碱性强,错误。故选C。

【题目】课本第二单元课题3制取氧气,课后作业中有“寻找新的催化剂”的探究内容,实验中学探究小组据此设计了如下探究方案。
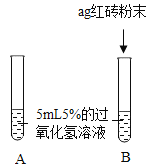
(提出问题)红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
(实验探究)
实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象, B中产生大量能使带火星木条复燃的气体 | ①产生的气体是____ ② 红砖粉末能改变过氧化氢分解速率 |
Ⅱ. 向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ① 又产生大量能使带火星木条复燃的气体 ② 滤渣质量等于ag | 红砖粉末的____和____在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
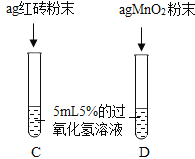
Ⅲ. | 两试管中均产生气泡 不同之处是________ | 红砖粉末的催化效果没有二氧化锰粉末好 |