题目内容
【题目】文文想通过实验测定稀硫酸中硫酸的质量分数,他分四次向182.5g稀硫酸(包含硫酸和水)中加入含有杂质的锌粉(杂质不溶于盐酸也不与盐酸发生反应),记录所加锌粉质量与产生氢气的质量如图。
次数 | 1 | 2 | 3 | 4 |
锌粉质量/g | 5 | 5 | 5 | 5 |
氢气质量/g | M | 0.15 | 0.1 | 0 |
(1)M的数值为.________ 。
(2)请计算稀硫酸中硫酸所占的质量分数_______。
(3)含杂质的锌中锌的质量分数_______。
【答案】0.15 10.7% 97.5%
【解析】
(1)根据题目中表格的信息可知,第四次加入锌粉,没有气体生成,说明硫酸完全消耗了,第三次加入5g锌粉,生成0.1g氢气,第二次加入5g锌粉,生成0.15g氢气,说明第三次加入5g锌粉后,硫酸已经消耗完了,那么一开始时,在硫酸过量条件下,每加入5g锌粉,生成0.15g氢气,M的数值为0.15g。
(2)182.5g稀硫酸生成氢气的质量为前三次加入锌粉生成氢气的质量之和。m(H2)=0.15g+0.15g+0.1g=0.4g;
设:总共消耗硫酸的质量为y。
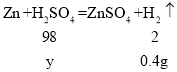
![]()
解得:y=19.6g
稀硫酸中硫酸所占的质量分数=![]() ;
;
答:稀硫酸中硫酸所占的质量分数为10.7%。
(3)设:第一次反应消耗锌的质量为x。
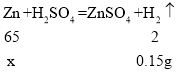
![]()
x=4.875g
含杂质的锌中锌的质量分数=![]()
答:含杂质的锌中锌的质量分数为97.5%。

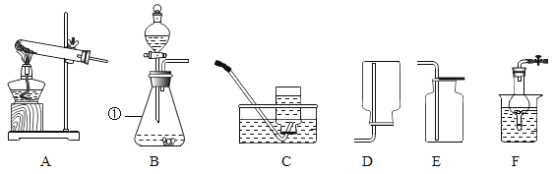
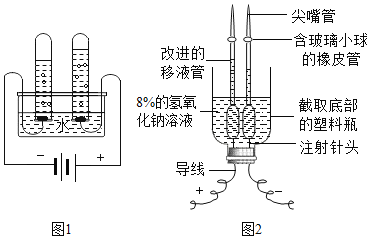
【题目】二百多年前,法国化学家拉瓦锡用图1装置定量的研究了空气的成分。仿照这个历史上著名实验的原理,用图2所示装置来测定空气中氧气的含量。

(实验回顾)图2是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。写出红磷燃烧的符号表达式_____。
(分析讨论)用红磷燃烧的方法测出的氧气含量总是低于21%,有没有其他物质可以代替红磷进行实验而使实验结果更准确呢?
(实验改进1)同学们用蜡烛代替红磷测定空气中氧气的含量,发现蜡烛很快熄灭,回流到集气瓶中的水远远小于瓶中气体体积的1/5。是什么原因所致呢?
(猜想与假设)猜想①:蜡烛燃烧产生CO2气体;猜想②:_____。
(实验验证)将蜡烛点燃后用氧气传感器定量测定瓶中的氧气含量,数据如图3。
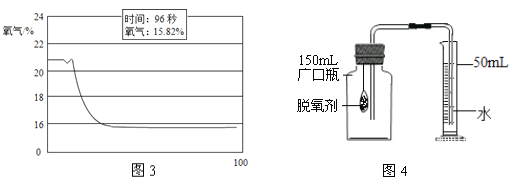
(得出结论)空气中氧气体积分数降低了_____%。
(查阅资料)在老师的指导下,同学们查阅了红磷、白磷、蜡烛等可燃物燃烧所需要的最低含氧量以及其他信息如下:
资料1:
可燃物名称 | 红磷 | 白磷 | 蜡烛 |
最低含氧量/% | 8.0 | 4.0 | 16.0 |
甲、乙、丙三个小组分别用过量红磷、白磷、蜡烛进行该实验,用测氧气浓度的传感器测得反应后的氧气浓度分别为8.85%、3.21%、16.7%,数据与表中的理论值基本一致。其中蜡烛燃烧后用测一氧化碳浓度传感器测算一氧化碳浓度约为2%。
资料2:二氧化碳因与氢氧化钠溶液发生化学反应,实验室常用氢氧化钠溶液来吸收二氧化碳。
资料3:蜡烛或者木炭在密闭的集气瓶中燃烧,氧气浓度不断变小的同时,会有一氧化碳气体生成。常温下一氧化碳难溶于水,且不与氢氧化钠溶液反应。
(交流与讨论)根据以上信息回答下列问题:
①白磷和红磷相比,使用白磷能使结果更准确,其原因是_____。
②有同学提议选用木炭替代红磷做实验,在集气瓶底部预先放少量氢氧化钠溶液吸收生成的二氧化碳气体,小华觉得不可行,其主要原因是_____。
(实验改进2)食品脱氧剂(以铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态。同学们尝试用图4装置进行实验来测定空气中氧气的含量。
下表是实验过程中记录的有关数据:
实验所需的时间/min | 0 | 5 | 10 | 30 | 35 | 45 |
量筒中液面的刻度/mL | 50 | 35 | 27.5 | 19.7 | 19.7 | 19.7 |
①脱氧剂发生复杂的化学反应,首先是铁粉与氧气、水反应生成氢氧化亚铁固体,写出该反应的符号表达式_____。
<>②分析表中数据得知,至少经过_____分钟后,量筒中的液面不再下降。③根据表中实验数据进行推算,广口瓶中氧气的体积分数约为_____(结果精确到0.1%)。
(实验拓展)铁在不同的条件下与氧气反应可生成不同种铁的氧化物, 58g四氧化三铁与多少克氧化铁(Fe2O3)中所含铁元素质量相等?_____(写出计算过程)
(实验评价)与燃烧红磷法相比,用脱氧剂测定空气中氧气含量的优点是_____。