题目内容
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)用化学符号表示:2个氮原子______;构成氯化钠的阳离子______。
(2)“玉兔”在月球岩石中发现了铁橄榄石(主要成分是Fe2SiO4),铁橄榄石中硅元素的化合价是+4价,则铁橄榄石中铁元素的化合价是______。
(3)某反应的微观示意图如图所示:
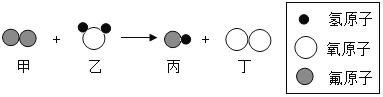
参加反应的甲物质和生成的丙物质分子数目比为___________。
【答案】2N Na+ +2 1:2
【解析】
(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故2个氮原子表示为:2N.
构成氯化钠的阳离子是钠离子,钠离子可表示为:Na+;
(2)铁橄榄石中硅元素化合价是+4,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(+4)+(-2)×4=0,则x=+2价.
(3)在点燃条件下,甲和乙反应生成丙和丁,由反应前后分子变化的微观示意图,该反应是氟分子和水分子反应生成氟化氢分子和氧气分子,反应的化学方程式为:2F2+2H2O═4HF+O2,参加反应的甲物质和生产的丙物质分子数目比为2:4=1:2。

【题目】文文想通过实验测定稀硫酸中硫酸的质量分数,他分四次向182.5g稀硫酸(包含硫酸和水)中加入含有杂质的锌粉(杂质不溶于盐酸也不与盐酸发生反应),记录所加锌粉质量与产生氢气的质量如图。
次数 | 1 | 2 | 3 | 4 |
锌粉质量/g | 5 | 5 | 5 | 5 |
氢气质量/g | M | 0.15 | 0.1 | 0 |
(1)M的数值为.________ 。
(2)请计算稀硫酸中硫酸所占的质量分数_______。
(3)含杂质的锌中锌的质量分数_______。
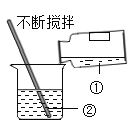
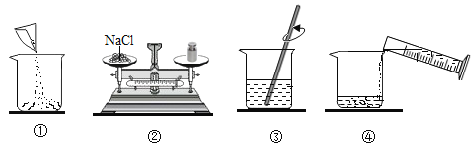
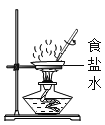
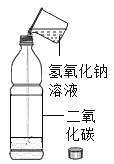
【题目】(一)小明在实验室观察完品红扩散实验后,想把变红的水做一个简单的处理后再排入下水道。请根据如图相关信息,回答下列问题:
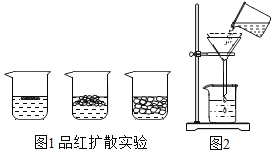
(1)图2过滤操作中必须用到的玻璃仪器分别是______、______、烧杯,请指出该操作过程中的其中两处错误______、______。
(2)小明同学将红色液体按过滤的正确操作完成后,发现过滤后的液体中仍有少量品红固体,则造成这种情况可能的原因是(填一种即可)______
(3)水是一种重要的资源,人类离不开水。在很长一段时期内,人类不了解水到底是由什么组成的。直到18世纪末,人类通过电解水实验才最终认识了水的组成。下列实验也能证明水是由氧元素和氢元素组成的是______(填序号)
A 氢气在氧气中燃烧 B 石蜡在空气中燃烧 C 水的蒸发 D 水的净化
(二)实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的文字表达式:______。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
(提出猜想)除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
(完成实验)按下表进行试验:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | KClO3 | 580 |
② | KClO3、MnO2(质量比1:1) | 350 |
③ | KClO3、CuO(质量比l:1) | 370 |
④ | KClO3、Fe2O3(质量比1:1) | 390 |
(分析数据、得出结论)
(1)由实验______形成对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是______。
(反思)
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后质量和______;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证______。