题目内容
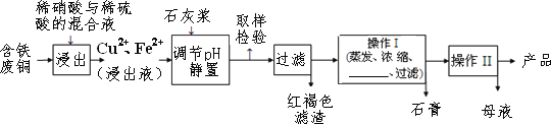
【题目】硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H 2O)和副产物石膏(CaSO4·2H 2O)的生产流程示意图:
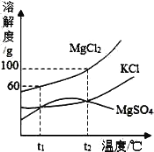
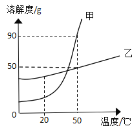
胆矾和石膏在不同温度下的溶解度(g/100g 水)如表。
温度(℃) | 20 | 40 | 60 | 80 | 100 |
石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红褐色滤渣的主要成分是_________;
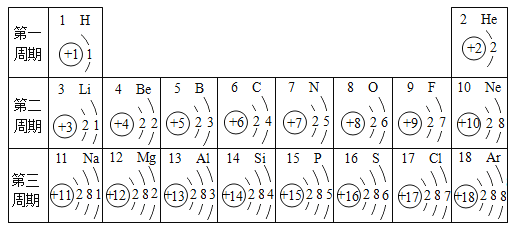
(2)含铁的废铜和稀硫酸反应的化学方程式_____
(3)操作 I 最后温度应该控制在_____℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、_____、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是_____。
【答案】Fe(OH)3 Fe+H2SO4=FeSO4+H2↑ 100 冷却结晶 减少因晶体溶解造成的损失
【解析】
(1)由工艺流程图转化关系可知,浸出液中加入石灰浆调节pH值,铁离子转化为Fe(OH)3沉淀析出,红褐色滤渣的主要成分为Fe(OH)3;
(2)铁和硫酸反应生成硫酸亚铁和氢气;化学方程式为:Fe+H2SO4=FeSO4+H2↑;
(3)由表中溶解度关系可知,胆矾溶解度随温度升高增大,而石膏的溶解度随温度升高降低,所以应控制在较高的温度,温度应该控制在100℃,制备的胆矾相对较纯;
(4)从溶液中分离出硫酸铜晶体应为将热溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥;硫酸铜易溶于水而不易溶于酒精,晶体用无水乙醇作洗涤液而不用蒸馏水是为了减少晶体溶解损失。

练习册系列答案
相关题目