题目内容
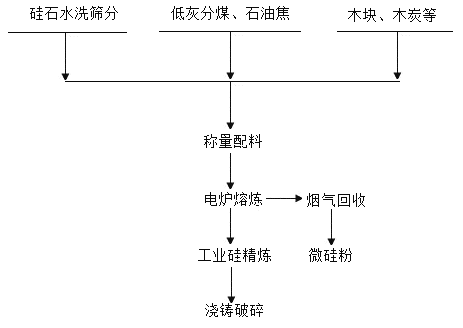
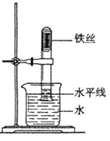
【题目】某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了如图两个实验:
组合序号 | ① | ② | ③ |
组合的溶液 | H2SO4 NaOH | H2SO4 NaCl | H2SO4 Na2CO3 |
实验二


实验二
[实验一]:把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液
(1)写出混合后得到蓝色沉淀一定发生反应的化学方程式_____。
(2)混合后所得无色溶液中一定含有的溶质是_____(填化学式,下同)可能含有的溶质是_____。
[实验二]:
(3)在组合①、②、③中,组合_____无明显现象,但它们的实质不同,为了证明实质不同。小夕在实验过程中使用了酚酞试液
(4)实验结束后把3个组合反应后的溶液混合,混合后溶液也显无色。混合后所得溶液中除酚酞外溶质的组成可能是_____(填化学式)
[结论]:
(5)复分解反应发生的条件是:生成物中有_____。
【答案】![]() NaC1、Na2SO4 NaOH ①② ①Na2SO4、NaC1、H2SO4;②Na2SO4、NaC1 沉淀、气体或水
NaC1、Na2SO4 NaOH ①② ①Na2SO4、NaC1、H2SO4;②Na2SO4、NaC1 沉淀、气体或水
【解析】
(1)把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液,说明蓝色沉淀是试管①中剩余的氢氧化钠与试管②中生成的氯化铜反应生成的,故反应的化学方程式写为:CuCl2+2NaOH=Cu(OH)2↓+2NaCl。
(2)氯化铜与氢氧化钠反应生成氢氧化铜沉淀与氯化钠,所以混合后所得无色溶液中一定含有的溶质是氯化钠,其化学式为NaCl,试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀,并没有白色沉淀,说明试管②中的氯化钡没有剩余,则试管②中生成的硫酸钠就留在溶液中,所以混合溶液中还一定有硫酸钠,其化学式为Na2SO4,故填NaCl、Na2SO4;
氢氧化钠与硫酸铜和氯化铜均能反应生成蓝色沉淀,所以溶液中可能有氢氧化钠剩余,其化学式为NaOH,故填NaOH。
(3)在组合①中的硫酸与氢氧化钠发生中和反应生成硫酸钠和水,没有明显的现象变化,组合②中的硫酸与氯化钠不发生反应,无明显现象,组合③硫酸与碳酸钠反应生成硫酸钠、水和二氧化碳,产生气泡,所以在组合①、②、③中,无明显现象变化的是①②,故填①②。
(4)3个组合反应后的溶液混合,混合后溶液也显无色,说明能够使酚酞试液变红色的氢氧化钠和碳酸钠没有剩余,则混合溶液中一定存在的是氯化钠和反应生成的硫酸钠,溶液中的酚酞不变红,则混合溶液中还可能含有硫酸,即溶质的存在形式有两种:①Na2SO4、NaC1、H2SO4②Na2SO4、NaC1,故填①Na2SO4、NaC1、H2SO4;②Na2SO4、NaC1。
(5)复分解反应发生的条件是生成物中有沉淀、气体或水生成,故填沉淀、气体或水。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案【题目】为验证“加热碳酸氢铵”所发生的变化和产物,两同学分别用甲、乙所示装置进行实验。

(1)甲实验中的现象是_______________。
(2)乙实验中试管口略向下倾斜的原因是_______________。乙实验中烧杯内反应化学方程式为_______________;实验中棉花逐渐变红色,则可说明反应产物中有_______________;相对于甲实验来说,乙实验的优点有(写一条)_______________。
(二)将一定量的K2CO3溶液与BaCl2溶液混合,过滤反应后的混合物。某兴趣小组的同学们欲探究滤液中溶质的组成。请你一同参与探究并回答有关问题:
[查阅资料]K2CO3溶液显碱性; BaCl2、 KCl溶液显中性。
[提出猜想]猜想1:滤液溶质是KCl;
猜想2:滤液溶质是_______________。
猜想3:滤液溶质是KCl和K2CO3。
[实验探究]
实验操作 | 实验现象 | 实验结论 |
① 取少量滤液于试管中,滴几滴无色酚酞试液,振荡 | 无明显现象 | ①猜想_________不成立 |
② 另取少量滤液于另一支试管中,滴加K2CO3溶液 | ______________ | ②猜想2成立。 写出相关的化学方程式 _____________ |
[问题讨论]小丽同学认为要证明猜想2成立也可改用AgNO3溶液,你认为小丽同学不能达到实验目的,你的理由是_______________。
[反思拓展]实验结束后,组内同学认为K2CO3是盐而其水溶液却显碱性,这可能与它的构成微粒有关,微粒符号是_______________。