题目内容
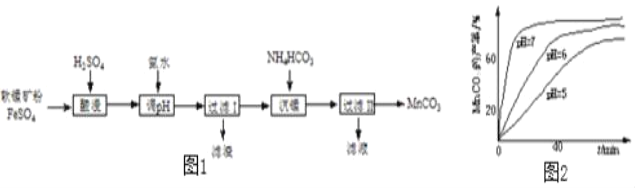
【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业作出了突出的贡献。他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱。表格中是几种物质在不同温度时的溶解度:
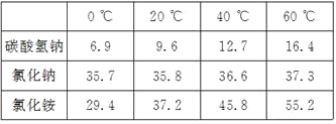
(1)从表中数据可以看出,温度对_____的溶解度影响不大。
(2)要使氯化铵饱和溶液中的氯化铵结晶析出,在____(填“较高”或“较低”)温度下进行比较合适。
(3)写出“侯氏制碱法”制碳酸氢钠的方程式_____。
(4)有人认为侯氏制碱法的优点有四:
A 生产过程中部分产品可选为起始原料使用
B 副产品是一种可利用的氮肥
C 反应不需要加热
D副产物不会造成污染环境
你认为其中正确的是___。
【答案】氯化钠 较低 NH3+H2O+CO2+NaCl===NaHCO3↓+NH4Cl ABD
【解析】
(1)从表中可以看出,温度对NaHCO3和NH4Cl的溶解度的影响都比较大,而对NaCl的溶解度影响不大,故选氯化钠。
(2)随着温度的升高,NH4Cl的溶解度变大,且受温度变化影响大,故可以通过在较高温度下配制NH4Cl的饱和溶液,然后再降温,结晶析出NH4Cl的办法将NH4Cl从溶液中分离出来。(3)侯氏制碱的原理:先将氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,故化学方程式:NaCl+NH3+H2O+CO2===NaHCO3↓+NH4Cl。
(4)根据氨碱法制纯碱的实验原理进行分析,以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱。先使氨气通入饱和食盐水中而成氨盐水,再通入二氧化碳生成溶解度较小的碳酸氢钠沉淀和氯化铵溶液,即NaCl+NH3+H2O+CO2===NaHCO3↓+NH4Cl。将经过滤、洗涤得到的NaHCO3微小晶体,再加热煅烧制得纯碱产品。A项,烧制时放出的二氧化碳气体可回收循环使用,含有氯化铵的滤液与石灰乳混合加热,所放出的氨气可回收循环使用,正确;B项,副产品是氯化铵,其中含有氮元素,是一种氮肥,正确;C项,碳酸氢钠分解制纯碱时需要加热,错误;D项,氯化铵是一种氮肥,可再利用,不是污染物,正确。故选ABD。

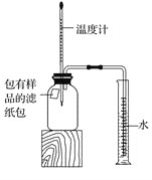
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后瓶中残留废液进行探究。
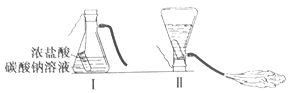
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是______。
(讨论与交流)
小明认为猜想I无需验证就知道是错误的,他的理由是_____(请用化学方程式说明)。
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论____(填“正确”或“错误”),理由是______________。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________________ | __________________ | 猜想3正确 |
(2)验证猜想4,可选择的试剂有____________。
A.酚酞溶液B.氢氧化钾溶液C.稀硫酸D.氯化钡溶液
(拓展与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行____操作,即可从废液中得到NaCl固体。
【题目】1kg不同燃料燃烧产生CO2和SO2的质量如表所示。
燃料 | 燃烧产物质量/g | |
CO2 | SO2 | |
汽油 | 2900 | 5.0 |
天然气 | 2500 | 0.1 |
煤 | 2500 | 11.0 |
①其中较清洁的燃料是______,使用______做燃料时最易形成酸雨。
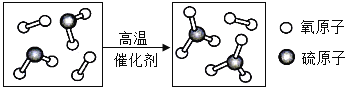
②酸雨形成过程中某一步反应的微观示意图如下图所示。则该反应的化学方程式为______。