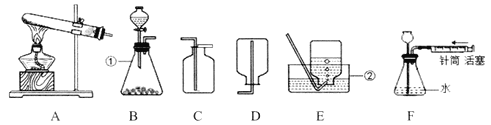
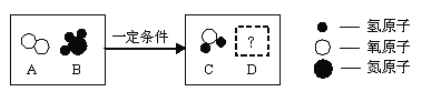
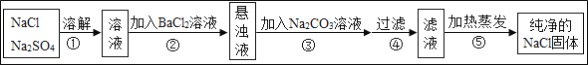题目内容
【题目】以软锰矿粉(主要含MnO2,还有少量Fe2O3)为原料制取MnCO3的流程如图1.
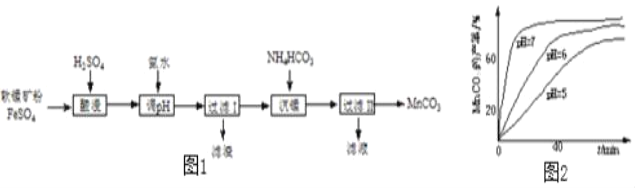
(1)“酸浸”时发生的反应有2FeSO4+MnO2+2H2SO4=_____+MnSO4+2H2O和_____。
(2)“过滤Ⅰ”所得滤渣的主要成分是_____。
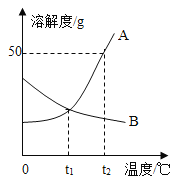
(3)“沉锰”时测得MnCO3的产率与溶液pH、反应时间t的关系如图2,反应要控制pH=_____,其理由是_____、_____。
(4)“过滤Ⅱ”所得滤液中溶质的主要成分是_____。
(5)为测定某软锰矿中MnO2的质量分数,称取2.0 g软锰矿样品,加入3.35 g草酸钠(Na2C2O4)固体,再加足量稀硫酸(杂质不参加反应),充分反应后,过量的Na2C2O4用31.6 g/L KMnO4溶液进行反应,当滴入10.0 mL KMnO4溶液时恰好完全反应。
已知:①MnO2+Na2C2O4+2H2SO4=MnSO4 +2CO2↑+2H2O+Na2SO4 ;②2KMnO4+5Na2C2O4+8H2SO4=2MnSO4+5Na2SO4+K2SO4+10CO2↑+8H2O.
求该软锰矿中MnO2的质量分数。_____(相对分子质量:KMnO4 158;Na2C2O4 134;MnO2 87)
【答案】Fe2(SO4)3 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O Fe(OH)3 7 时间相同时,MnCO3的产率最高 MnCO3产率相同时,所需时间最短;(或者简单答成:产率高、速度快) (NH4)2 SO4 87%
【解析】
(1)由于软锰矿粉(主要含MnO2,还有少量Fe2O3),所以“酸浸”时发生的反应是氧化铁和硫酸反应生成硫酸铁和水,以及硫酸亚铁和二氧化锰以及硫酸反应生成硫酸铁和硫酸镁以及水,对应的化学方程式为:2FeSO4+MnO2+2H2SO4=Fe2(SO4)3+MnSO4+2H2O和 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O。
(2)由于后续得到的是含锰化合物,所以过滤操作中分离出的应该是含铁化合物,而过程是和氨水反应得到且酸浸过程中生成的是三价铁的化合物,所以“过滤Ⅰ”所得滤渣的主要成分是难溶性的 Fe(OH)3。
(3)根据“沉锰”时测得MnCO3的产率与溶液pH、反应时间t的关系图,可知反应要控制pH=7,其理由是 时间相同时,MnCO3的产率最高、MnCO3产率相同时,所需时间最短。
(4)过滤II前是硫酸锰和碳酸氢铵反应生成碳酸锰和溶液,根据质量守恒定律,可知溶液的成分为硫酸铵,所以“过滤Ⅱ”所得滤液中溶质的主要成分是 (NH4)2SO4。
(5)当滴入10.0 mL KMnO4溶液时恰好完全反应,则消耗的高锰酸钾的质量为31.6 g/L×10.0 mL×1L/1000mL=0.316g
设与高锰酸钾反应的草酸钠的质量为x
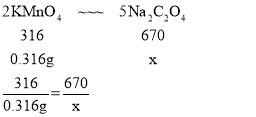
x=0.67g
则与二氧化锰反应的草酸钠的质量为3.35g﹣0.67g=2.68g
设该软锰矿中MnO2的质量分数为y
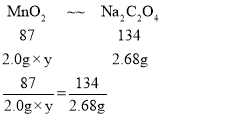
y=87%
故答案为:
(1)Fe2(SO4)3;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(2)Fe(OH)3;(3)7; 时间相同时,MnCO3的产率最高; MnCO3产率相同时,所需时间最短;(或者简单答成:产率高、速度快);(4)(NH4)2 SO4;(5)87%。

 阅读快车系列答案
阅读快车系列答案