题目内容
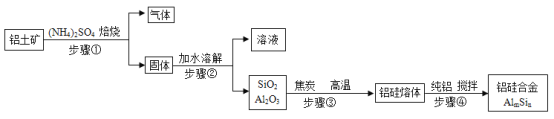
【题目】用铝土矿(主要含SiO2、Al2O3和少量Fe2O3等)制取铝硅合金材料有干法、湿法等方法,其中干法制备的工艺流程如图所示。
(已知:I.SiO2不溶于水、不与硫酸反应。Ⅱ.转化率是反应物转化为生成物的百分率。)
(1)铝硅合金的硬度比纯铝的硬度_______。
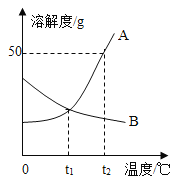
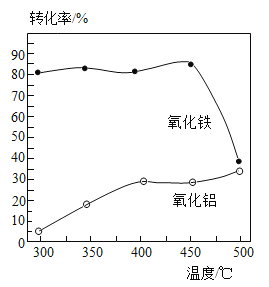
(2)步骤①中焙烧除铁的反应为:4(NH4)2SO4+Fe2O3![]() 2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为_______℃。
2NH4Fe(SO4)2+3H2O+6NH3↑(Al2O3部分发生类似反应,SiO2不发生类似反应)。已知Fe2O3、Al2O3转化为硫酸盐的转化率与温度的关系如图所示,则焙烧除铁最适宜的温度为_______℃。
(3)步骤②中包括加水溶解、_______、洗涤等操作。
(4)步骤③中利用焦炭还原SiO2、Al2O3会产生中间体SiC、Al4C3.写出高温下Al4C3与Al2O3反应生成A1和CO的化学方程式:_______。
(5)若用湿法处理铝土矿,加过量的硫酸浸取,所得溶液中的阳离子有_______。
【答案】大 300 过滤 Al4C3+Al2O3![]() 6Al+3CO Al3+、Fe3+、H+
6Al+3CO Al3+、Fe3+、H+
【解析】
(1)合金的硬度一般大于其组成金属的硬度,所以铝合金的硬度比纯铝的硬度大;
(2)根据硫酸盐的转化率与温度的关系图提供信息可知,300℃时,焙烧除铁转化率最高,所以焙烧除铁最适宜的温度为300℃;
(3)步骤②分离难溶性固体与可溶性固体,包括加水溶解、过滤、洗涤等操作;
(4)高温下Al4C3与Al2O3反应生成A1和CO,反应的化学方程式为:Al4C3+Al2O3![]() 6Al+3CO;
6Al+3CO;
(5)氧化铝与硫酸反应生成硫酸铝和水;氧化铁与硫酸反应生成硫酸铁和水,所以用湿法处理铝土矿,加过量的硫酸浸取,所得溶液中的阳离子有Al3+、Fe3+、H+。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目