题目内容
【题目】水是生命之源,是最常见的溶剂。
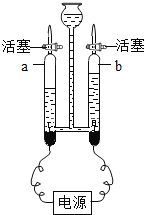
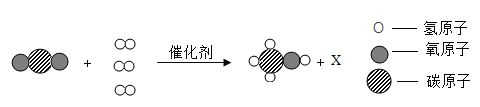
①上图为电解水实验装置,负极产生的气体是_______,检验b管中气体的方法是_______;
②在水电解器中加入100g含有少量NaOH的水(已知NaOH可以加快水的电解速度,电解时NaOH不发生变化,其他损失忽略不计),若通电一段时间后,溶液质量减少了4.8g,则电解过程中得到的氧气的物质的量为________(根据化学方程式计算)。
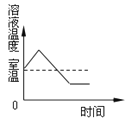
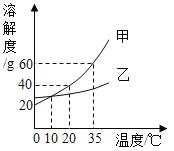
③甲、乙两种固体物质溶解度曲线如图所示,回答问题:

Ⅰ. t1℃时,甲的溶解度_____乙的溶解度(填“>”或“<”或“=”);
Ⅱ.将t1℃乙的不饱和溶液变成饱和溶液的方法:_____(写一种);
Ⅲ.将20克甲放入t2℃的50克水中,充分溶解后所得溶液的质量为_______g;
Ⅳ.在盛有等质量t2℃蒸馏水的两支试管中,分别加入等质量的甲和乙,充分振荡后,试管底部均有未溶解的固体,再将两支试管降温到t1℃。在两支试管由t2℃到t1℃的变化过程中,下列说法正确的是____
a两支试管中剩余的固体均增加 b t1℃两支试管中剩余固体的质量相同
c甲乙溶液的溶质质量分数均减小 d t1℃时甲乙溶液均为饱和溶液
【答案】氢气 将燃着的木条放在b管尖嘴口,打开活塞,木条燃烧得更旺,说明该气体是氧气 0.13mol = 增加乙物质或恒温蒸发溶剂 65 bd
【解析】
①在电解水实验中,“正氧负氢”,故负极产生的气体是氢气;电解水时,产生氢气和氧气的体积比约为2∶1,由图可知,b管中产生的气体是氧气,检验氧气的方法:将燃着的木条放在b管尖嘴口,打开活塞,木条燃烧得更旺,说明该气体是氧气;
②溶液质量减少了4.8g,说明水的质量减少了4.8g,即4.8g水在通电的条件下反应生成氢气和氧气,设电解过程中得到的氧气的质量为x

![]() x≈4.27g
x≈4.27g
电解过程中得到的氧气的物质的量为:![]() ≈0.13mol;
≈0.13mol;
③Ⅰ.由图可知,t1℃时,甲的溶解度曲线与乙的溶解度曲线相交,说明t1℃时,甲的溶解度=乙的溶解度;
Ⅱ.t1℃乙的不饱和溶液变成饱和溶液的方法有:增加乙物质或恒温蒸发溶剂;
Ⅲ.由图可知,t2℃时,甲物质的溶解度为30g,即该温度下,100g水中最多能溶解30g甲物质,故50g水最多能溶解15g甲物质,故将20克甲放入t2℃的50克水中,充分溶解后所得溶液的质量为:65g;
Ⅳ.a、由图可知,甲的溶解度随温度的升高而增加,乙的溶解度随温度的升高而减小,故将两支试管降温到t1℃,甲的溶解度降低,剩余固体质量增加,乙的溶解度增加,剩余固体质量减小,不符合题意;
b、由图可知,t1℃时,甲的溶解度=乙的溶解度,故该温度下,在盛有等质量蒸馏水的两支试管中,分别加入等质量的甲和乙,剩余固体的质量相同,符合题意;
c、由图可知,甲的溶解度随温度的升高而增加,乙的溶解度随温度的升高而减小,故将两支试管降温到t1℃,甲的溶解度降低,析出的晶体质量变大,溶质质量分数减小,乙的溶解度增加,析出的晶体质量变小,溶质质量分数增加,不符合题意;
d、t2℃时,试管底部均有未溶解的固体,这时甲、乙均为饱和溶液,降温后,甲的溶解度降低,故甲还是饱和溶液;降温后,乙的溶解度增加,且t1℃时,甲的溶解度=乙的溶解度,即该温度下,100g水中最多能溶解的甲物质和乙物质的质量相同,相同质量的水中,溶解的甲物质和乙物质质量相同,加入甲、乙物质的质量相同,此时甲是饱和溶液,故乙也是饱和溶液,符合题意。故选bd。

 智能训练练测考系列答案
智能训练练测考系列答案【题目】化学实验兴趣小组的学生用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水。
实验步骤 | 实验现象 | 实验结论 |
分别用a、b、c三支试管取样,各加入一定量碳酸钠溶液 | a中有气泡产生 | a中物质是稀盐酸 |
b中无明显现象 | b中物质是食盐水 | |
c中____________________ | c中物质是澄清石灰水 |
写出a试管中发生反应的化学方式___________________。
把c试管反应后的物质进行过滤,得到滤液。(提出问题)滤液中溶质的成分是什么?
猜想一: Na2CO3和NaOH;
猜想二: NaOH;
猜想三:___________________。
(实验过程)为证明猜想一是否正确,进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取一定量滤液于试管中,加入一种盐溶液(写溶质化学式)________________ | 有白色沉淀 | 猜想一正确 |
同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值,发现a试管中的废液显酸性,从环保、经济、操作简便等方面考虑,应向废液加入(写化学式)____________后再排放。