题目内容
(8分)某学习小组围绕“气体的实验室制取”进行研讨,请你参与完成下面的问题。

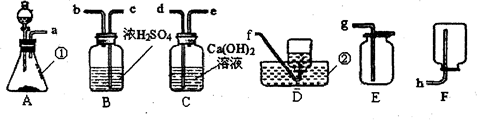
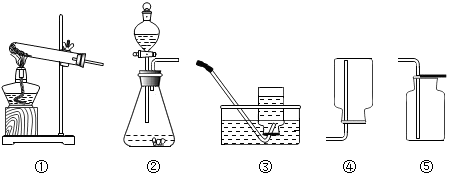
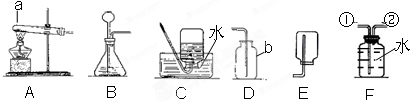
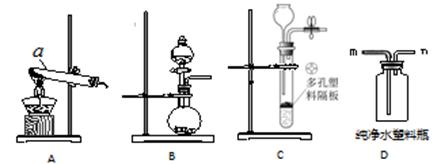
(1)图①装置制取气体的适用条件是 。
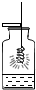
(2)图③装置相比图②装置的主要优点是 。
(3)实验室不宜用镁来代替锌与稀H2SO4反应制取H2,主要原因是
。
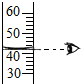
(4)实验室若用图④装置收集NH3时,气体应从 端通入。(填字母)

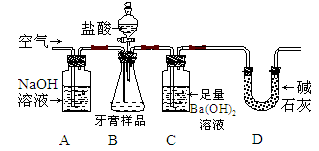
(5)为了测定铜元素的相对原子质量Ar(Cu),某同学以氢气还原氧化铜的反应设计了:
上图中第一个装有碱石灰的U形管的作用是 。
若测得反应前氧化铜的质量为ag,实验完成后第二个装有碱石灰的
U形管增加的质量为bg,则Ar(Cu)= 。(用a、b表示)。
(6)请利用单孔橡胶塞、玻璃导管、胶皮管、试管、集气瓶和玻
璃片,设计一套制取CO2的实验装置,并将该实验装置的简图画在
答题卡的方框内。


(1)图①装置制取气体的适用条件是 。
(2)图③装置相比图②装置的主要优点是 。
(3)实验室不宜用镁来代替锌与稀H2SO4反应制取H2,主要原因是
。
(4)实验室若用图④装置收集NH3时,气体应从 端通入。(填字母)

(5)为了测定铜元素的相对原子质量Ar(Cu),某同学以氢气还原氧化铜的反应设计了:
上图中第一个装有碱石灰的U形管的作用是 。
若测得反应前氧化铜的质量为ag,实验完成后第二个装有碱石灰的
U形管增加的质量为bg,则Ar(Cu)= 。(用a、b表示)。
(6)请利用单孔橡胶塞、玻璃导管、胶皮管、试管、集气瓶和玻
璃片,设计一套制取CO2的实验装置,并将该实验装置的简图画在
答题卡的方框内。

(1)反应物是固体,反应需要加热 (2)能随时控制反应的开始和结束
(3)镁与稀H2SO4反应速率太快,不利于实验操作 (4)b
(5)吸收氢气中的水蒸气 18a/b-16
(6)
(3)镁与稀H2SO4反应速率太快,不利于实验操作 (4)b
(5)吸收氢气中的水蒸气 18a/b-16
(6)

试题分析:(1)图①装置适用于反应物是固体,反应条件为加热的反应来制取气体。
(2)图③装置当打开时,液体药品进入试管中。当液面超过塑料板时与固体接触,可反应生成气体。当关闭开关时,装置内的气压增大,将液体药品压入漏斗中,液面低于塑料板时,反应即停止。因此图③装置能随时控制反应的开始和结束,而装置②无法实现这种目的。
(3)镁与稀H2SO4反应速率太快,不利于实验操作。所以不适合在实验室中来制取H2。
(4)氨气的的密度比空气小,适合用向下排空气法收集。所以实验室若用图④装置收集NH3时,气体应从b端通入,将空气从开口在下方的a管排出。
(5)碱石灰是固体氢氧化钠与生石灰的混合物,可用于除去水蒸气。所以第一个装有碱石灰的U形管的作用是吸收氢气中的水蒸气。
实验完成后第二个装有碱石灰的U形管增加的质量,即为氢气与氧化铜反应生成水的质量。设铜的相对原子质量为x,根据反应前后氧元素的质量不变,可列式为:ag×(
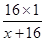 ×100%)=bg×(
×100%)=bg×(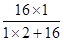 ×100%)解之得x=18a/b-16。
×100%)解之得x=18a/b-16。(6)根据所给的仪器,可采用稀盐酸和大理石石反应来制取二氧化碳气体。由于二氧化碳的密度比空气大,所以应采用向前排空气法收集。二氧化碳可溶解于水,不可用排水法。所以装置为

练习册系列答案
相关题目
 过滤
过滤