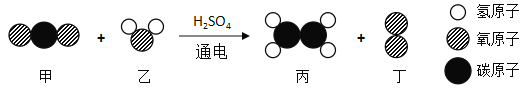
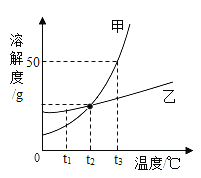
题目内容
【题目】小明在收拾实验室时发现有一瓶没有盖瓶盖的氢氧化钙固体,报告老师后,老师告诉同学们这瓶固体可能已经变质了。于是小明和小组的同学们一起探究这瓶久置于空气中的氢氧化钙固体的成分。
(提出问题):久置于空气中的氢氧化钙固体的成分?
(猜 想):猜想 1:氢氧化钙 猜想 2:碳酸钙 猜想 3:_______
(实验验证):
实验步骤 | 实验现象 | 实验结论 |
(1)取少量固体样品于试管中,加入一定的水振荡,静置 | ||
(2)取步骤(1)中的上层清液,滴加 2-3 滴无色酚酞试液,振荡 | ______ | 样品中含有氢氧化钙 |
(3)往上面试管中的剩余固体中倒入足量的稀盐酸 | ______ | 样品中含有碳酸钙 |
(得出结论):猜想 3 正确
(实验反思):上述实验中产生气泡的化学方程式为:______
(拓展提升):进一步探究这瓶氢氧化钙固体的变质程度,计算固体样品中氢氧化钙的质量分数?
(实验设计):小明和同学们设计了如下图所示的实验装置来测定样品中氢氧化钙的质量分数(铁架台、 铁夹等在图中均已省略)
(资料):饱和碳酸氢钠溶液可以吸收盐酸挥发出来的 HCl 气体;碱石灰为 NaOH 和 CaO 的混合物;装置 F 用于吸收空气的气体
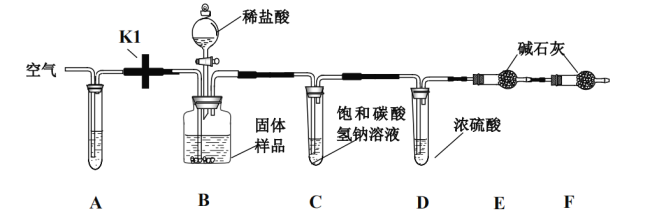
(实验步骤):
①准确称量 10.0g 固体样品装入装置 B
②将装置 B 分别与 A、C、D 连接,打开开关 K1,从 A 处鼓入空气,几分钟后,将开关 K1 关闭,再将已 称量过的干燥管 E、F 与 D 连接
③打开 B 中分液漏斗的活塞,再向 B 中缓缓的注入足量的稀盐酸
④待完全反应后,再次打开开关 K 缓缓鼓入空气几分钟,最后称量干燥管 E,增重 1.1g
(实验分析)
(1)已知装置 A 中试剂为某种碱性溶液,其作用是为了吸收空气中的某气体,写出吸收该气体所发生的
化学反应方程式:______________,实验前第一次鼓入空气是为了驱赶装置中的该气体,若反应后不鼓入空气,对测定结果的影响是_____________(填“偏大”或“偏小”)
(2)D 装置的作用是_____。
(3)根据干燥管 E 增加的质量,可推算出样品中氢氧化钙的质量分数为_______。
(4)实验结束后,同学们认为反应后的酸性废液不能直接进行排放,应该进行处理以后再排放,正确的处理方法是加入过量的______
A 熟石灰 B 碳酸钙 C 生石灰 D 氢氧化钠
【答案】氢氧化钙和碳酸钙 溶液变红色 产生大量的气泡 ![]()
![]() 偏大 吸收水(干燥 CO2 ) 75% B
偏大 吸收水(干燥 CO2 ) 75% B
【解析】
1、[猜 想]:有三种情况,没有变质,部分变质,完全变质。
猜想 1:氢氧化钙 猜想 2:碳酸钙 猜想 3:氢氧化钙和碳酸钙
2、[实验验证]:
(1)取少量固体样品于试管中,加入一定的水振荡,静置;
(2)酚酞遇碱变成红色,取步骤(1)中的上层清液,滴加 2-3 滴无色酚酞试液,振荡酚酞变成红色,样品中含有氢氧化钙;
(3)碳酸钙和稀盐酸反应生成氯化钙、二氧化碳、水,往上面试管中的剩余固体中倒入足量的稀盐酸,产生气泡,样品中含有碳酸钙。
3、[实验反思]:上述实验中产生气泡的化学方程式为:![]()
4、[实验分析]
(1)已知装置 A 中试剂为某种碱性溶液,其作用是为了吸收空气中的某气体,以免干扰二氧化碳的质量,装置 A 中试剂为某种碱性溶液是氢氧化钠溶液,氢氧化钠吸收二氧化碳所发生的化学反应方程式:![]() ;实验前第一次鼓入空气是为了驱赶装置中的该气体,若反应后不鼓入空气,装置中有二氧化碳气体,根据二氧化碳计算的碳酸钙质量偏小,氢氧化钙质量分数偏大;
;实验前第一次鼓入空气是为了驱赶装置中的该气体,若反应后不鼓入空气,装置中有二氧化碳气体,根据二氧化碳计算的碳酸钙质量偏小,氢氧化钙质量分数偏大;
(2)D 装置的浓硫酸具有吸水性,作用是干燥二氧化碳。
(3)最后称量干燥管 E,增重 1.1g,说明生成二氧化碳1.1g。
设样品中氢氧化钙的质量分数为x。
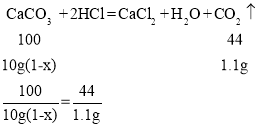
x=75%
(4)实验结束后,同学们认为反应后的酸性废液不能直接进行排放,应该进行处理以后再排放,正确的处理方法是加入过量的碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、二氧化碳、水,过量的碳酸钙不会污染环境;如果加入过量的熟石灰、生石灰、氢氧化钠,溶液变成碱性,不符合环保要求。
故选B。

【题目】化学链燃烧是新的燃烧概念,即燃料不直接与空气接触燃烧,而是以载氧体(如CaSO4等)在两个反应器之间的循环来实现燃料的燃烧过程(如图1)。请回答下列问题:
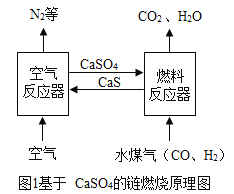
(1)空气反应器中主要发生化合反应,化学方程式为_____。燃料反应器中, CO与CaSO4发生的反应方程式为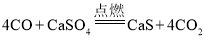 。
。
(2)实验室模拟CO与石膏(CaSO4﹒2H2O)的反应,并测定CO与石膏(CaSO4﹒2 H2O)是否反应完全,设计装置如图2。
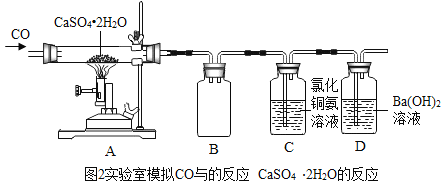
①广口瓶B的作用是_____。C中反应的化学方程式为![]() _____
_____![]() ,C装置的作用是_____,该实验的尾气无毒。
,C装置的作用是_____,该实验的尾气无毒。
②完成实验报告(已知:热的CaS会跟氧气反应;氯化亚铜和氨水混合溶液为无色)。
实验步骤 | 现象 | 分析与解释 |
检查气密性并装填好药品后,首先应先通一会CO | C中_____(填反应现象) | |
点燃A处酒精喷灯 | D中_____(填反应现象) | |
停止加热,继续通一会CO,直到装置冷却 | 继续通CO目的:(1)使生成的CO2全部被氢氧化钡溶液吸收; (2)_____ | |
取A中残留固体,加足量稀盐酸 | _____(填反应现象),有少量不溶物 |
|
(3)若所取石膏样品(CaSO4﹒2 H2O)质量为1.00g,装置D中产生的BaCO3的质量为3.94g,求石膏样品的转化率。_____(转化率:![]() ,己知BaCO3的相对分子质量为197)(写出计算过程)
,己知BaCO3的相对分子质量为197)(写出计算过程)
(4)D装置中不宜使用澄清石灰水的理由是_____。