题目内容
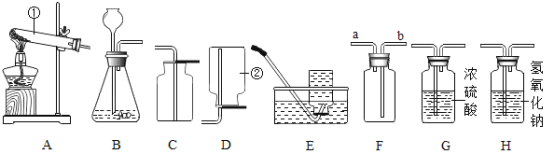
【题目】暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源于铁粉的氧化。有同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为250mL)中的水的体积为45mL(铁粉生锈消耗的水忽略不计)。下列说法错误的是( )

A. 实验前必须检査装置的气密性
B. 若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足
C. 通过本次实验数据测得空气中氧气的体积分数约为19.6%
D. 不用等温度计读数恢复至实验前的温度就可以记录量筒内剩余水的体积
【答案】D
【解析】
A、实验前必须检査装置的气密性,故选项正确;
B、若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足,氧气不能完全反应,故选项正确;
C、本次实验数据测得空气中氧气的体积分数约为:![]() ×100%≈19.6%,故选项正确;
×100%≈19.6%,故选项正确;
D、应该等温度计读数恢复至实验前的温度才可以记录量筒内剩余水的体积,这是因为反应放热,气体体积膨胀,会导致进入集气瓶中的水的体积偏少,从而导致实验结果偏小,故选项错误。故选D。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】小明在收拾实验室时发现有一瓶没有盖瓶盖的氢氧化钙固体,报告老师后,老师告诉同学们这瓶固体可能已经变质了。于是小明和小组的同学们一起探究这瓶久置于空气中的氢氧化钙固体的成分。
(提出问题):久置于空气中的氢氧化钙固体的成分?
(猜 想):猜想 1:氢氧化钙 猜想 2:碳酸钙 猜想 3:_______
(实验验证):
实验步骤 | 实验现象 | 实验结论 |
(1)取少量固体样品于试管中,加入一定的水振荡,静置 | ||
(2)取步骤(1)中的上层清液,滴加 2-3 滴无色酚酞试液,振荡 | ______ | 样品中含有氢氧化钙 |
(3)往上面试管中的剩余固体中倒入足量的稀盐酸 | ______ | 样品中含有碳酸钙 |
(得出结论):猜想 3 正确
(实验反思):上述实验中产生气泡的化学方程式为:______
(拓展提升):进一步探究这瓶氢氧化钙固体的变质程度,计算固体样品中氢氧化钙的质量分数?
(实验设计):小明和同学们设计了如下图所示的实验装置来测定样品中氢氧化钙的质量分数(铁架台、 铁夹等在图中均已省略)
(资料):饱和碳酸氢钠溶液可以吸收盐酸挥发出来的 HCl 气体;碱石灰为 NaOH 和 CaO 的混合物;装置 F 用于吸收空气的气体
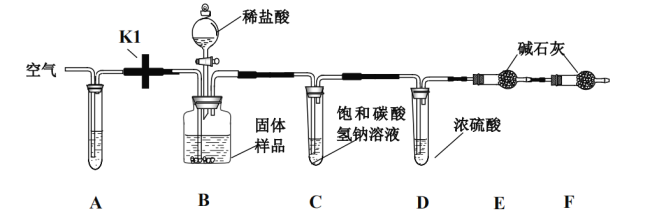
(实验步骤):
①准确称量 10.0g 固体样品装入装置 B
②将装置 B 分别与 A、C、D 连接,打开开关 K1,从 A 处鼓入空气,几分钟后,将开关 K1 关闭,再将已 称量过的干燥管 E、F 与 D 连接
③打开 B 中分液漏斗的活塞,再向 B 中缓缓的注入足量的稀盐酸
④待完全反应后,再次打开开关 K 缓缓鼓入空气几分钟,最后称量干燥管 E,增重 1.1g
(实验分析)
(1)已知装置 A 中试剂为某种碱性溶液,其作用是为了吸收空气中的某气体,写出吸收该气体所发生的
化学反应方程式:______________,实验前第一次鼓入空气是为了驱赶装置中的该气体,若反应后不鼓入空气,对测定结果的影响是_____________(填“偏大”或“偏小”)
(2)D 装置的作用是_____。
(3)根据干燥管 E 增加的质量,可推算出样品中氢氧化钙的质量分数为_______。
(4)实验结束后,同学们认为反应后的酸性废液不能直接进行排放,应该进行处理以后再排放,正确的处理方法是加入过量的______
A 熟石灰 B 碳酸钙 C 生石灰 D 氢氧化钠