题目内容
【题目】某校化学兴趣小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或加热的条件下均不反应.那么,铜与浓硫酸能否发生反应呢?他们设计了如下图所示装置进行探究.
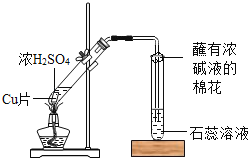
[猜想与假设]
①在常温下能反应
②常温下不能反应,但在加热条件下能反应
③在加热条件下不能反应
[查阅资料]
含有Cu2+的水溶液通常显蓝色
[实验与事实]
操作①将一小块铜片放入试管中,加入足量浓硫酸,无明显现象;
操作②加热该试管,铜片上有气泡,产生了有刺激性气味的气体;
操作③停止加热,将试管中的残液慢慢倒入水中,溶液呈蓝色.
[分析与思考]
(1)甲同学认为,由以上探究可知:猜想_____(填序号)是正确的.
(2)乙同学认为,经检验产生的气体是SO2,所以铜跟浓硫酸在加热条件下反应的产物只是SO2和CuSO4.
(3)丙同学认为,在实验装置中,“蘸有浓碱液棉花”的作用是_____.
[反思与评价]
(4)操作③中,从安全角度考虑_____(填“可以”或“不可以”)将水倒入残液中,其理由是_____.
(5)在[分析与思考](2)中对产物只是SO2和CuSO4的判断是否准确_____(填“是”或“否”),其理由是_____.
[拓展与应用]
(6)根据以上探究和已掌握的知识,该兴趣小组的同学设计了两个用铜制取硫酸铜的实验方案:
①Cu![]() CuSO4; ②Cu
CuSO4; ②Cu![]() CuO
CuO![]() CuSO4
CuSO4
经过对两种方案的讨论、对比,同学们认为方案②具有的优点有_____(填序号),所以工业上制备硫酸铜不是直接利用浓硫酸与铜反应.
A提高铜的利用率 B提高硫酸的利用率
C不产生污染大气的SO2 D不用浓硫酸,安全性好
【答案】② 吸收SO2 不可以 残液中含有浓硫酸,若将水倒入残液中,浓硫酸溶于水放出大量的热,会使溶液飞溅. 否 反应物中有氢元素,但二氧化硫和硫酸铜中都不含氢元素. BC
【解析】
[分析与思考]
(1)根据实验操作和现象,可以证明铜和浓硫酸在加热的时候能反应,生成物中有二氧化硫和硫酸铜;
(3)二氧化硫有毒,能和碱溶液反应,所以可以用浓碱液吸收;
[反思与评价]
(4)浓硫酸溶于水会放出大量的热,造成液滴飞溅,所以不能把含浓硫酸的物质倒入水中;
(5)因为反应物中有氢,硫、氧、铜四种元素,根据反应前后元素的种类不变的原则,生成物中应该有氢元素;
[拓展与应用]
比较这两个方案,从经济,环保,安全的角度考虑,浓硫酸腐蚀性太强,使用时要注意安全,二氧化硫有毒等,通过综合考虑,方案②比①要好的多。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】在高温下,铁与水蒸气能发生反应生成一种常见铁的氧化物和一种气体,某化学 学习小组的同学对此反应甩感兴趣,在小组集体协作下设计了如下实验,以探究铁粉与水蒸气反应后的产物,也邀请你一起来完成下列探究:
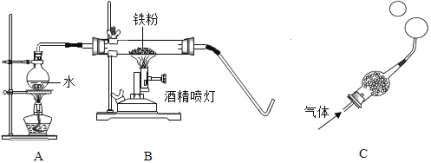
(1)A装置的作用是___;
(2)探究生成的气体是什么?
(猜想与假设)猜想一:生成的气体可能是氢气;
猜想二:生成的气体可能是氧气;
(实验探究)将生成的气体通入C装置,球形管里装有碱石灰干燥剂,导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡,当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
(推断)生成的气体是___.
(3)探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被进磁铁吸引 | 否 | 否 | 能 |
能否与盐酸反应 | 能 | 能 | 能 |
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引.
(猜想与假设)猜想一:剩余固体是Fe和Fe3O4;
猜想二:剩余固体是:___.
(实验探究)
实验操作 | 实验现象及结论 |
____ | _____ |
[实检结论]铁与水蒸气反应的化学方程式为:___.
(反思与交流)该黑色固体不可能是FeO、Fe2O3,理由是___.
【题目】聪聪同学在实验室帮老师整理废弃药品时发现一瓶没有标签的绿色粉末,对其组成很好奇.征得老师允许后,设计了以下实验进行探究.
操作步骤 | 实验现象 | 结论或化学反应方程式 |
取少量样品置于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连. | ①产生大量气体,使石灰水变浑浊. ②样品全部溶解,溶液呈蓝色. | ①样品中含有_____离子 ②样品中含有_____离子 |
在上述蓝色溶液中,插入一根洁净的铁丝. | ①铁丝表面缓缓产生少量气泡. ②片刻后铁丝表面出现红色物质. | ①_____ ②_____ (均用方程式表示) |
为了进一步确定该物质的元素组成,查阅部分资料后,他继续进行了实验.
[资料查阅]白色的无水硫酸铜可做吸水剂,遇水会变成蓝色.
[实验步骤]
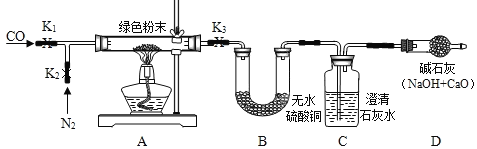
①如图搭建实验仪器,并检验装置的气密性.
②在A装置中装入11.1g绿色粉末.关闭K1,打开K2、K3,持续通入适量N2.
③关闭K2、K3,分别称量装置B、C、D的质量,记录数据.
④打开K3,点燃酒精灯加热绿色粉末直至装置C中无气泡产生时,关闭K3,熄灭酒精灯.分别称量装置B、C、D的质量,记录数据.
⑤待A冷却后,打开K1、K3,持续通入适量CO,再次点燃酒精灯加热.
⑥当A中粉末全部变红后,熄灭酒精灯.试管冷却后,关闭K1.称量装置A、B、C、D的质量,记录数据.
[实验现象和数据处理]
装置A | 装置B | 装置C | 装置D | |
第一次 加热后 | 绿色粉末变黑色 | _____ 质量增加0.9g | 出现白色沉淀, 质量增加2.2g | 无明显变化 质量不改变 |
第二次 加热后 | 黑色粉末变红色 质量为6.4g | 无明显变化, 质量不改变 | 沉淀先增加后部分溶解; 质量增加 | 无明显变化 质量不改变 |
[实验分析与反思]
1、老师看了实验方案后认为,从环保的角度来看,此装置有一个缺陷,建议装置D后还应添加一个酒精灯,并在实验步骤_____(填实验步骤的序号)中点燃.
2、步骤②通入氮气的目的是:_____.
[实验结论]该绿色粉末的组成元素是:_____;各元素的质量比为:_____(写出计算过程)

