题目内容
【题目】请结合图示实验装置,回答下列问题:
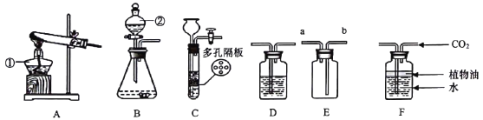
(1)写出仪器②的名称____________
(2)用高锰酸钾制氧气选用的发生装置是________(选填序号),反应的化学方程式为_______
(3)若B装置中固体为锌粒,②中加入_______试剂可制得氢气,要获得干燥的氢气,应先将气体通过盛有______的D装置,再用E装置收集,气体应端通入________(选填“a”或“b ”)。
(4)实验室可用B或C装置制取二氧化碳,反应的化学方程式为____,C相对于B装置的优点有_____
(5)若用F装置收集二氧化碳,植物油的作用是___________
【答案】分液漏斗 A 2KMnO4![]() K2MnO4+MnO2+O2↑ 稀硫酸 浓硫酸 a 2HCl+CaCO3
K2MnO4+MnO2+O2↑ 稀硫酸 浓硫酸 a 2HCl+CaCO3![]() CaCl2+H2O+CO2↑ 可以控制反应的发生和停止 防止二氧化碳与水接触
CaCl2+H2O+CO2↑ 可以控制反应的发生和停止 防止二氧化碳与水接触
【解析】
(1)仪器②的名称为:分液漏斗;
(2)加热高锰酸钾制氧气应选用加热固体制取气体装置,故选用的发生装置是A,反应的化学方程式为2KMnO4![]() K2MnO4+MnO2+O2↑ ;
K2MnO4+MnO2+O2↑ ;
(3)实验室中常用锌与稀硫酸反应制取氢气,故若B装置中固体为锌粒,②中加入稀硫酸试剂可制得氢气;浓硫酸具有吸水性,且不与氢气反应,可用于干燥氢气,故要获得干燥的氢气,应先将气体通过盛有浓硫酸的D装置;氢气的密度比空气小,故用E装置收集,应使空气从b端逸出,气体从a端通入;
(4)实验室常用石灰石与稀盐酸反应制取二氧化碳,反应的化学方程式为2HCl+CaCO3![]() CaCl2+H2O+CO2↑;C装置有多孔隔板,可以控制反应的发生和停止;
CaCl2+H2O+CO2↑;C装置有多孔隔板,可以控制反应的发生和停止;
(5)二氧化碳溶于水也能与水反应,不能直接用排水法收集二氧化碳,用F装置收集二氧化碳,植物油的作用是防止二氧化碳与水接触。

【题目】下列实验不能达到实验目的的是( )
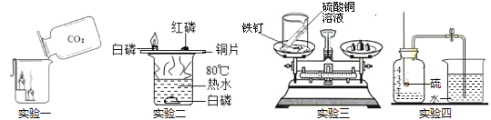
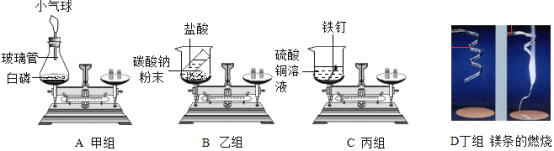
A. 实验一验证二氧化碳密度大于空气,不支持燃烧且不具备燃烧
B. 实验二探究燃烧需要的条件
C. 实验三探究质量守恒定律
D. 实验四测量空气中氧气所占的体积分数
【题目】在浓硫酸催化作用下,固体草酸(H2C2O4)受热分解生成水和气体.某化学课外兴趣小组对所得气体成分进行了探究.
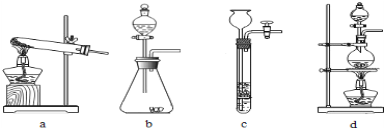
(1)下列可用作草酸分解制取气体的装置是_____________(填字母编号)
(提出问题)如何通过实验确定气体成分.
(猜想)
猜想1 | 猜想2 | 猜想3 |
只有CO | 只有______ | CO、CO2都有 |
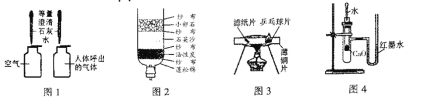
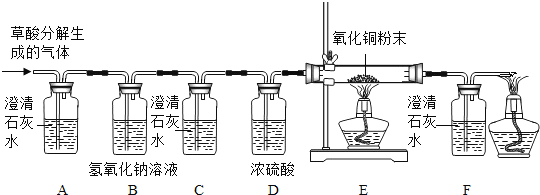
(设计)基于猜想3,兴趣小组同学设计了如图装置:
(信息提供)
①氢氧化钠溶液能很好的吸收二氧化碳。
②浓硫酸是实验室里一种常用的干燥剂,能干燥某些气体。
(探究)
(1)实验过程中观察到装置_________(填字母)中澄清石灰水变浑浊,证明有CO2气体。其反应方程式为 ________。
(2)实验过程中除了观察E装置中黑色粉末变成红色外,还应该观察到;_____,证明有CO气体。
(结论)通过探究证明:猜想3成立.草酸分解化学方程式是__________。
(讨论)
(1)C装置作用是 ________, D装置作用是____________
(2)装置末端酒精灯的作用是______________
(提升)
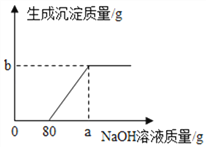
若反应结束后,F处的澄清石灰水质量增加了8.8克,则参加反应的氧化铜的质量是多少________?若F处吸收的CO2先通过下列变化:CO2→CO→CO2(每步反应都进行完全),再将得到的CO2通入足量的澄清石灰水,理论上会生成_______g沉淀。