题目内容
【题目】为测定某稀硫酸的溶质的质量分数,小兰同学设计了如下实验方案.
![]()
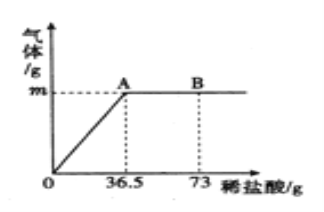
第②步实验中生成沉淀的质量与加入NaOH溶液的质量关系如图.
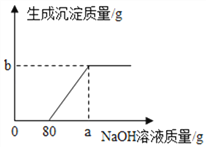
(1)分析第②步实验:与先加入的80g NaOH溶液反应的物质是_____(填化学式),继续加入NaOH溶液后产生的沉淀是_____(填名称)
(2)计算稀硫酸的溶质的质量分数______________(写出计算过程)
【答案】 H2SO4 氢氧化铜 9.8%
【解析】(1)氧化铜和硫酸反应后生成物中一定有硫酸铜,可能有剩余的硫酸,当向硫酸和硫酸铜的混合物中加入氢氧化钠溶液时,氢氧化钠先和硫酸(H2SO4)反应生成硫酸钠,后与硫酸铜反应生成氢氧化铜沉淀,与硫酸反应的氢氧化钠的质量是80g×10%=8g;
设与氢氧化钠反应的硫酸质量为x
2NaOH+ H2SO4 = Na2SO4+2H2O
80 98
8g x
![]() x=9.8g
x=9.8g
设与氧化铜反应的硫酸质量为y
CuO + H2SO4 = CuSO4+H2O
80 98
8g y
![]() y=9.8g
y=9.8g
稀硫酸的溶质的质量分数=![]()
答:(1). H2SO4 (2). 氢氧化铜 (3). 9.8%

练习册系列答案
相关题目