题目内容
【题目】在浓硫酸催化作用下,固体草酸(H2C2O4)受热分解生成水和气体.某化学课外兴趣小组对所得气体成分进行了探究.
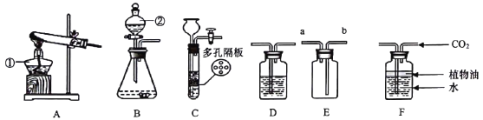
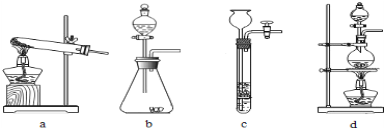
(1)下列可用作草酸分解制取气体的装置是_____________(填字母编号)
(提出问题)如何通过实验确定气体成分.
(猜想)
猜想1 | 猜想2 | 猜想3 |
只有CO | 只有______ | CO、CO2都有 |
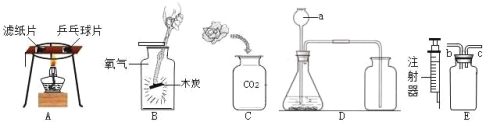
(设计)基于猜想3,兴趣小组同学设计了如图装置:
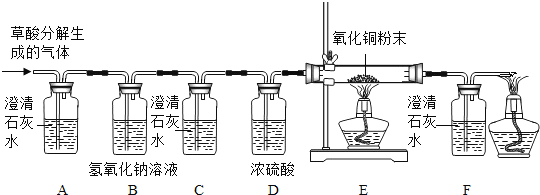
(信息提供)
①氢氧化钠溶液能很好的吸收二氧化碳。
②浓硫酸是实验室里一种常用的干燥剂,能干燥某些气体。
(探究)
(1)实验过程中观察到装置_________(填字母)中澄清石灰水变浑浊,证明有CO2气体。其反应方程式为 ________。
(2)实验过程中除了观察E装置中黑色粉末变成红色外,还应该观察到;_____,证明有CO气体。
(结论)通过探究证明:猜想3成立.草酸分解化学方程式是__________。
(讨论)
(1)C装置作用是 ________, D装置作用是____________
(2)装置末端酒精灯的作用是______________
(提升)
若反应结束后,F处的澄清石灰水质量增加了8.8克,则参加反应的氧化铜的质量是多少________?若F处吸收的CO2先通过下列变化:CO2→CO→CO2(每步反应都进行完全),再将得到的CO2通入足量的澄清石灰水,理论上会生成_______g沉淀。
【答案】d CO2 A CO2 + Ca(OH)2 == CaCO3↓+ H2O F中澄清石灰水变浑浊 H2C2O4═H2O+CO↑+CO2↑ 证明二氧化碳已经被除尽 干燥一氧化碳 防止污染空气 16g 40g
【解析】
(1)由题中信息可知,可用作草酸分解制取气体的装置是d,猜想2为:二氧化碳,
【探究】
(1)实验过程中观察到装置A中澄清石灰水变浑浊,证明有CO2气体。其反应是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,方程式为 CO2 + Ca(OH)2 == CaCO3↓+ H2O;
(2)一氧化碳和氧化铜加热条件下反应生成铜和二氧化碳,实验过程中除了观察E装置中黑色粉末变成红色外,还应该观察到F中澄清石灰水变浑浊,证明有CO气体。
【结论】
通过探究证明:猜想3成立.草酸分解化学方程式是:H2C2O4═H2O+CO↑+CO2↑;
【讨论】
(1)C装置作用是通过澄清石灰水不变浑浊证明二氧化碳已经被除尽, 排除原有二氧化碳对一氧化碳验证的影响,D装置作用是干燥一氧化碳,
(2)装置末端酒精灯的作用是_点燃尾气中的一氧化碳,防止污染空气;
【提升】
若反应结束后,F处的澄清石灰水质量增加了8.8克,说明生成二氧化碳8.8g,设参加反应的氧化铜的质量是x,

![]() x=16g
x=16g
若F处吸收的CO2先通过下列变化:CO2→CO→CO2(每步反应都进行完全),
CO2 + C ![]() 2CO 2CO+O2
2CO 2CO+O2 ![]() 2CO2,转化后二氧化碳的质量为17.6g
2CO2,转化后二氧化碳的质量为17.6g
再将得到的CO2通入足量的澄清石灰水,设得碳酸钙的质量为y
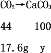
![]() y=40g
y=40g
即理论上会生成40g沉淀

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案