��Ŀ����
ijС��ͬѧ��������������ƣ�����ͼ���кͷ�Ӧ����̽����������룮
��ͬѧ��װ������������Һ���ձ��м������ᣬ�����������ۣ���������δ������Ӧ��
��ͬѧ����з�̪������������Һ���Թ��������μ����ᣬ��Һ���� ��ɫ��Ϊ��ɫ�����ۣ��������ʷ����˷�Ӧ����Ӧ�Ļ�ѧ����ʽΪ�� ����
�����Ϊ�ҵ�ʵ��֤���������������Ʒ������кͷ�Ӧ�����Լ�ʵ�����̽����
[�������]��ʵ������Һ����ʲô���ʣ�
[��������]����һ��ֻ��CaCl2���������CaCl2��Ca��OH��2������������CaCl2��HCl��
[ʵ��̽��]Ϊ��֤���룬��ͬѧ����˷���1�ͷ���2��������������ʵ�飮
| ������� | ����1 | ����2 | ����3 |
| ʵ��������ֱ�ȡ������ʵ������Һ���Թ��У� |  | 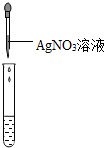 |  |
| ʵ������ | �Աȱ���ɫ����pH��7 | ������ɫ���� | |
| ʵ����� | ��Һ����HCl | ��Һ����CaCl2 |
[ʵ������]����ʵ������ͷ������в���֮�����䲻��֮������ ����
������ۺ�ͨ������3��֤���˲�������ȷ����ʵ����Ӧ�۲쵽������Ϊ�� ����
[ʵ����չ]Ϊ��Լ��Դ�ͱ���ʵ���Һ�Ի�����Ⱦ��С��ͬѧ������1�ͷ���3����ʵ����ձ���ʣ����Һ��ϣ����ʱδ�������������Ի��Һ�е��η�����գ��뽫������������±���
| Ҫ������� | �����Լ� | ��Ҫ���� |
| �� �� | �� �� | �� �� |
�죻Ca��OH��2+2HCl=CaCl2+2H2O��
[ʵ������]������1��ʹ��pH��ֽ�IJ������ԣ�����2�м�AgNO3������ɫ����˵����Һ����Cl��������˵��ֻ���Ȼ��ƣ�����������������а�ɫ�������ɣ�
[ʵ����չ]��Ҫ������� �����Լ� ��Ҫ���� CaCl2��NaCl Na2CO3��HCl ������м���Na2CO3��Һ�����ٲ������������ˣ�����Һ��������NaCl�������˺�Ĺ����ϡ���������ٲ������壬����Һ������������CaCl2
���������������̪��Һ��������Һ�Ժ�ɫ����������з�̪������������Һ���Թ��������μ����ᣬ��Һ�ɺ�ɫ��Ϊ��ɫ��˵���������ʷ����˷�Ӧ����������������Һ�����ᷴӦ�����Ȼ��ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪCa��OH��2+2HCl=CaCl2+2H2O��
[ʵ������]����pH��ֽ�ⶨ��Һ�����ʱ���ܽ�pH��ֱֽ���������Һ�У����Է���1��ʹ��pH��ֽ�IJ������ԣ�����2�м�AgNO3������ɫ����ֻ��˵����Һ����Cl��������˵��ֻ���Ȼ��ƣ�
����̼������Һ�����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�����Լ�̼������Һ���Ȼ�����Һ��Ӧ����̼��Ƴ��������Է���3��֤���˲�������ȷ����ʵ����Ӧ�۲쵽������Ϊ����������������а�ɫ�������ɣ�
[ʵ����չ]������1�ͷ���3����ʵ����ձ���ʣ����Һ��ϣ����ʱδ����������˵��û��̼���ƣ�������ʱ��Һ������Ϊ�Ȼ��ƺ��Ȼ��ƣ����Ȼ��ƺ��Ȼ��Ʒ�����Լ��������̼������Һ����ַ�Ӧ����ˣ�����Һ��������NaCl�������˺�Ĺ����ϡ���������ٲ������壬����Һ������������CaCl2��
���㣺�кͷ�Ӧ����Ӧ�ã���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��
��������Ͽα�֪ʶ��ʵ�鼼�ܣ�������ѧ���ķ������⣬�������������������ۺ��Խ�ǿ�������ѧ��������֪ʶ��ʵ�����ϵ�������������ѧ���Ĵ�����������һ���������ۺ��⣮

 ����Ӣ��ϵ�д�
����Ӣ��ϵ�д� ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д�ʵ��������ƿʧȥ��ǩ�İ�ɫ��ĩ����֪���ǿ�����̼��ơ�������þ��������е�һ�֡��������ʵ������������������������ʵ�鱨�森
| ʵ����� | Ԥ����������� |
| | |
| | |
ij��ѧ������ͬѧ�����ڽ����ᡢ���֪ʶ��̽���������ǽ�ѧƬ�ϣ�����������в�������д�ո�
��ѧ��ʵ�顿��������̼�ֱ�ͨ�����ʯ��ˮ������������Һ�У��۲쵽ǰ�߱���ǣ���������������
��ѧ�����ݡ�����ʯ��ˮ����ǵ�ԭ���� �����û�ѧ����ʽ��ʾ��
��������⡿������̼ͨ������������Һ�����������������Ƿ����˻�ѧ��Ӧ��
��������衿����٣����߷����˻�ѧ��Ӧ������ڣ�����û�з�����ѧ��Ӧ
��ʵ��̽����
��1��С���������ͼ��ʾ��A��B����ʵ�飮
ʵ������A��������ƿ���B���� ��
��2��С����ΪС����ʵ���ǿ��еģ��乲ͬԭ���Ƕ�����̼������������Һ��Ӧ��ʹ������ѹǿ���ͣ�С��ͬѧȴ�Դ�������ɣ�����ΪС����ʵ�鲻�Ͻ������������� ����Ҫ�õ���ѧ�Ͻ��Ľ��ۣ������ø�װ�ã������ĶԱ�ʵ������ ����
��3��С����Ƶ���ͨ����������������֤���룬�������дʵ�鱨�森
| ʵ�鲽�� | ʵ������ | ʵ����� |
| ��Bʵ������Һ�м��� �� �� | �� �� | ��֤�˶�����̼������������Һ��Ӧ |
����˼��չ��ͨ����̽��ʵ�飬���Ƿ��֣�����û����������Ļ�ѧ��Ӧ�����Դ�������ͬ�ĽǶ�֤����Ӧ�ķ������������Ƕ����� ������ ����
���в����У������л��ϳɲ��ϵ��ǣ�������
| A������ | B���� | C������ | D����˿ |





