题目内容
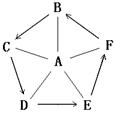
实验室有四瓶失去标签的溶液,现标为A、B、C、D,分别是碳酸钠溶液、氯化钡溶液、硫酸钠溶液和稀盐酸中的一种.
[提出问题]如何区分出四种溶液?
[进行实验]甲同学实验如图所示:由此甲同学认为A一定不是 
[表达与交流]甲同学向实验后的溶液中滴加酚酞溶液,酚酞溶液由无色变为红色,则甲同学的结论:A是氯化钡溶液.乙同学不同意甲同学的结论,乙同学的理由是 .
于是乙同学另取少量A于试管中,向其中滴加一种试剂是 溶液,
观察到的明显现象是 .由此证明了甲同学的结论是错误的.同时确定了A.乙同学继续实验如图所示:
[收集证据]观察到C中产生气泡,D中产生白色沉淀.
[解释与结论]写出D中发生反应的化学方程式
乙同学最终通过实验区分出了四种溶液.
[反思与评价]请指出甲同学区分上述四种溶液时,在实验方法上的一点不足之处 .
【进行实验】碳酸钠溶液或硫酸钠溶液;[表达与交流]若A是稀盐酸,氢氧化钡与稀盐酸反应后氢氧化钡过量,也能使酚酞溶液变红(或酚酞溶液变红只能说明实验后的溶液中有氢氧化钡,不能说明A是氯化钡溶液);碳酸钠溶液(或碳酸钾溶液;或紫色石蕊溶液);产生气泡(或产生气泡;或紫色石蕊溶液变为红色);
[解释与结论]H2SO4+BaCl2=BaSO4↓+2HCl;[反思与评价]甲同学在实验开始时只取A,没有同时取A、B、C、D进行对比实验是不科学的方法(或甲同学用实验后的溶液证明A,没有另取原溶液鉴别是错误的方法).
解析试题分析:【进行实验】由于氢氧化钡与碳酸钠反应生成碳酸钡沉淀,与硫酸钠反应生成硫酸钡沉淀,所以加入氢氧化钡没有现象,说明一定不是碳酸钠、硫酸钠;【表达与交流】若A是稀盐酸,氢氧化钡与稀盐酸反应后氢氧化钡过量,溶液显碱性也能使酚酞溶液变红;由于氯化钡与碳酸钠反应生成碳酸钡白色沉淀,所以如果加入碳酸钠,没有现象,说明不能是氯化钡;盐酸与碳酸钠反应生成氯化钠、水、二氧化碳,所以现象是有气泡产生;【解释与结论】D中产生白色沉淀.说明含有钡离子,即氯化钡,所以反应物是硫酸和氯化钡,生成物是硫酸钡和盐酸,用观察法配平即可;【反思与评价】甲同学在实验开始时只取A,没有同时取A、B、C、D进行对比实验是不科学的方法(或甲同学用实验后的溶液证明A,没有另取原溶液鉴别是错误的方法).
考点:酸、碱、盐的鉴别;酸碱指示剂及其性质;碱的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
点评:推断题是中考中必考的知识点,同学们要根据物质间的反应现象和反应规律进行推理判断,找到突破口,依次得出结论.

 天天练口算系列答案
天天练口算系列答案某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式 .
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是 .
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 .
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  |  |  |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出【实验探究】(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是 .
(2)实验方案中也有一个是错误的,错误的原因是 .
化学小组同学在加热二氧化锰样品时,发现有气泡产生(如图一所示),于是他们对这个异常现象进行了探究。
(1)对气体成分的探究:加热二氧化锰样品,用燃着的木条靠近试管口,木条熄灭。将气体通入澄清的石灰水,发现石灰水变浑浊,产生的气体是 。
(2)对气体来源的探究:
甲同学认为:该气体来自于试管中的空气,请你设计实验证明该假设不成立
| 实验步骤及现象 | 结论 |
| 加热空的试管,另一端的澄清石灰水没有变浑浊 | 假设 (填“不成立”或“成立”) |
乙同学认为:二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体。他设计了如图二所示的实验进行研究,其中B装置的作用是检验A中反应是否完全,B中的试剂是 ,实验中观察到D处澄清石灰水变浑浊。他又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现D处澄清的石灰水也变浑浊。通过乙同学的实验证明,二氧化锰中混有炭粉,炭粉与 反应产生了这种气体。
几年前,一辆载满20t电石的挂车,在浙江滨江区燃起熊熊大火并伴有大量黑烟.事故路面上洒落了五六百米燃着的石头.这辆货车在雨中整整燃烧了一天,消防官兵对大火也束手无措,场面让人震撼.大家对电石的化学性质产生了浓厚的兴趣,请你一起与他们完成下列探究活动.
【查阅资料】电石的主要成分是碳化钙(CaC2),可以与水反应生成一种可燃性气体及白色固体.常见的可燃性气体中,乙炔(C2H2)燃烧时伴有大量黑烟.
【猜想与假设】
电石与水反应生成的可燃性气体是:氧气、氢气或乙炔(C2H2);电石与水反应生成的白色固体是:氧化钙、氢氧化钙或碳酸钙.大家做出以上推断的理由是 .
大家讨论后一致认为该气体不可能是氧气,原因是 ,白色固体不可能是氧化钙,原因是(用化学方程式表示) .
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取适量电石加水反应,收集生成的气体,验纯后点燃. | 气体燃烧,产生黄色火焰并伴有浓烈黑烟. | 电石与水反应产生的气体是 |
| (2)取适量反应后生成的固体于试管中,滴加过量稀盐酸. | 固体溶解, . | 电石与水反应产生的固体不是碳酸钙 |
| (3)取适量反应后生成的固体于试管中加水,向上层清液中滴加2~3滴 . | 溶液变红 | 电石与水反应产生的固体是氢氧化钙 |
【反思交流】载有电石的货车可以在雨中整整燃烧一天而不熄灭,说明电石与水的反应是(填“吸热”或“放热”)反应.
某小组同学用盐酸和氢氧化钙,对酸和碱的中和反应进行探究.请你参与.
甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象.结论:两种物质未发生反应.
乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由 色变为无色.结论:两种物质发生了反应.反应的化学方程式为 .
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应.并对甲的实验继续探究.
[提出问题]甲实验后的溶液中有什么溶质?
[作出猜想]猜想一,只有CaCl2;猜想二有CaCl2和Ca(OH)2;猜想三,有CaCl2和HCl.
[实验探究]为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验.
| 方案编号 | 方案1 | 方案2 | 方案3 |
| 实验操作(分别取少量甲实验后的溶液于试管中) |  | 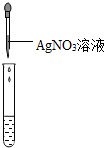 |  |
| 实验现象 | 对比标准比色卡:pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有HCl | 溶液中有CaCl2 |
[实验评价]丙的实验操作和方案中有不足之处,其不足之处是 .
大家讨论后通过方案3即证明了猜想三正确,其实验中应观察到的现象为 .
[实验拓展]为节约资源和避免实验废液对环境污染,小组同学将方案1和方案3及甲实验后烧杯中剩余溶液混合(混合时未见明显现象),并对混合液中的盐分离回收,请将相关内容填入下表.
| 要分离的盐 | 所用试剂 | 主要操作 |
| | | |