题目内容
【题目】氢氧化钙和氢氧化钠都是常用的碱。
(1)氢氧化钙溶液和氢氧化钠溶液中都含有大量的_____(填离子符号),所以化学性质相似。
(2)请写出氢氧化钙溶液与下列物质反应的化学方程式:
①与盐酸反应:_____;
②与碳酸钠溶液反应:_____;
③与二氧化碳反应:_____。属于碱的共同性质的是_____(填编号)。
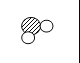
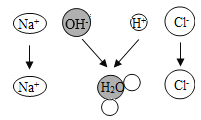
(3)氢氧化钠长期露置于空气中容易变质,所以NaOH要密封保存。如图表示一瓶完全变质的NaOH溶液,在变质前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号)。

![]() _____,
_____,![]() _____,
_____,![]() _____。
_____。
【答案】OH- Ca(OH)2+2HCl=CaCl2+2H2O Ca(OH)2+Na2CO3=CaCO3↓+2NaOH Ca(OH)2+CO2=CaCO3↓+H2O ①③ Na+ CO32- OH-
【解析】
(1)氢氧化钙溶液和氢氧化钠溶液中都含有大量的OH-,所以化学性质相似。
(2)①氢氧化钙溶液与盐酸反应生成氯化钙和水,反应的化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O。
②氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。
③氢氧化钙溶液与二氧化碳反应生成碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O。
碱能与酸发生中和反应,能与非金属氧化物反应生成盐和水,碳酸钠不能与氢氧化钠等碱溶液溶液反应,故属于碱的共同性质的是①③。
(3)变质前溶液中存在的主要离子是钠离子和氢氧根离子,完全变质NaOH溶液中含有钠离子、碳酸根离子等,故![]() 表示Na+;
表示Na+;![]() 表示CO32-;
表示CO32-;![]() 表示OH-。
表示OH-。

 阅读快车系列答案
阅读快车系列答案【题目】宏观、微观和符号之间建立联系是化学学科的待点。甲、乙、丙、丁、戊五种物质,它们的部分化学式和微观示意图分别列于下表中。
物质 | 甲 | 乙 | 丙 | 丁 | 戊 |
微观示意图 |
|
|
|
|
|
化学式 |
|
|
(1)用符号表示2个丁分子______,五种物质中,属于氧化物的是______![]() 用化学式表示
用化学式表示![]() ;
;
(2)工业上生产氢气的方法之一是利用甲、乙两种物质在高温、高压下生成丙和丁。而得到的丙物质又会随即与乙物质发生反应,生成丁和戊。通过这一系列反应,参加反应的甲和得到的丁质量比为______。